펄스 에너지원을 구동력으로 하는 마이크로젯 인젝터 개발 및 약물 주입 효능 평가
Copyright © The Korean Society for Precision Engineering
This is an Open-Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
A pulsed-power source has the advantage of releasing a peak power over a short time interval. In this study, we implemented two types of such energy source, namely laser and dielectric break down power sources. We built the high-pressure flow-output actuator utilizing such power sources in a micro-jet drug delivery system. We compared the jet speed from each power source and analyzed the drug penetration performance of the micro-jet injector. We found that hat the bubble growth rate caused by a dielectric breakdown power source per power input was three times faster than the laser power source. By using the micro-jet injector, we performed the insulin injection test using mouse models having diabetes mellitus to evaluate whether micro-jet injector has equivalent drug delivery performance when compared against conventional syringe-type injection.
Keywords:
Micro-jet, Underwater-spark discharge, Laser-induced bubble, Needle-free, Drug-delivery, Diabetes mellitus키워드:
마이크로젯, 수중 방전, 레이저 유도 버블, 무바늘, 약물 전달, 당뇨병1. 서론
종래 바늘식 주사기의 문제점을 해결하기 위한 약물 전달 기술이 시장 기술로서 도입되고 있으며 국내의 경우, 대기업을 중심으로 의료용 진단 및 분석 기술 개발이 주목을 받고 있다. 현재 허가 받은 분사식 주사기를 이용할 경우 피부를 뚫고 들어간 약물은 피하지방층까지 주입되므로, 피하지방층 까지만 전달되어도 효과가 있는 약물인 인슐린이나 백신, 호르몬제 등에 적합하다. 이 때문에 대부분의 연구 개발은 인슐린 환자들을 중심으로 널리 사용될 수 있는 개인용 장비 개발에 집중되고 있다. 고속 약물 마이크로젯(Micro-Jet)의 발생을 위해서는 피분사 약물에(직접 또는 간접적으로) 강한 추진력을 가하여 약물이 마이크로 노즐 분사구(Orifice)를 통해 강력하게 외부로 배출되도록 하여야 한다. 이러한 마이크로젯 약물 전달 시스템에서 추진력을 발생시키는 방식은 1930년대 이래로 다양하게 개발되어 왔는데, 최근까지 압전 세라믹 소자를 이용한 분사 방식,1 알루미늄 포일에 레이저 빔을 가함으로써 유발되는 충격파를 통한 분사방식,2 압축 스프링이나 압축 가스를 이용하는 방식,3 로렌츠 힘(Lorentz Force)을 이용한 분사 방식4 등의 다양한 분사 방식이 개발되었다. 하지만 이러한 분사 방식의 동력원은 젯 분사가 끝날 때까지 연속적으로 강한 파워를 출력한다. 이는 필요한 약물을 1회 스트로크(Stroke)에 모두 주입하여야 한다는 것이며, 예컨대 인슐린의 경우 0.2 cc의 약물을 1회 스트로크에 주입하면 한번에 많은 양의 약물이 피하 조직을 찢고 들어가 고통이 수반된다. 이를 해결하기 위한 동력원이 소량의 약물을 빠른 주기로 분사하는 펄스 파워 동력원이다. 이와 같은 동력원으로써 일정한 주기를 가지고 방출되는 고전력 펄스 레이저(Highly Powered Pulsed Laser), 액체 내 절연파괴(Underwater-Spark Discharge)5,6등이 있다. 이러한 동력원은 저장된 에너지를 짧은 순간에 방출하여 많은 양의 피크 파워(Peak Power)를 전달할 수 있다는 장점이 있다. 따라서 이러한 동력원을 통해 유체를 전달하는 메커니즘을 구현할 경우 소량의 고압 유동을 빠른 반복 주기로 분사할 수 있는 장점이 있다. 따라서 약물 주입 시 통증을 저감시킬수 있다.
본 연구는 펄스 형태의 파워 소스를 이용한 유동발생 메커니즘을 마이크로젯 약물 전달 시스템5-9에 적용하여 펄스 파워를 이용한 고출력의 유동발생기 개발의 가능성을 보임에 의미가 있다. 이러한 파워 소스로써 두 가지 형태의 파워 소스를 사용하였는데 레이저 에너지와 액체 내 절연파괴(Dielectric Breakdown)에 의한 에너지가 있다. 낮은 이라디언스 에너지(Irradiance Energy)를 가지는 레이저를 구동액에 조사할 경우 구동액의 한점에서 온도가 증가하며 갑작스런 증발에 의하여 증기 버블(Vapor Bubble)이 발생한다.10 이러한 버블은 250 μs의 시간 동안 팽창한다.8-11 구동액의 미소 면적에 고전압, 저전류의 전기에너지를 방전하면 스파크가 발생한다. 이를 액체 내 절연파괴현상이라고 한다.13 이러한 현상은 전극에 인가되는 전압이 전극 사이 물질의 절연파괴 전압(Break Down Voltage)보다 높을 경우 발생한다. 이 때 발생하는 스파크는 구동액을 이온화시키며 케비테이션 버블(Cavitation Bubble)을 발생한다.12
이러한 펄스 에너지를 통해 약물을 전달하는 메커니즘을 펄스레이저와 액체 내 절연파괴를 이용한 마이크로젯 약물 전달시스템에 적용하였다. 각 파워 소스에 따른 버블 팽창속도 및 젯 속도의 성능 변화를 비교하고 약물 전달에 적합한 파워소스가 전기식 절연 파괴 에너지임을 결정하였다. 또한 이러한 파워소스를 적용한 마이크로젯 인젝터가 피하 약물 투여의 기기로써 효능을 가지는지 여부를 확인하기 위하여 돼지 등심 조직과 돼지 복부 진피층에 약물을 침투 시킨 조직을 가시화하여 침투 깊이를 분석하였으며 당뇨를 유발시킨 마우스 모델에 인슐린을 주입하여 바늘식 주사기로 주입한 것과 동일한 약물 효능을 발생시키는지 여부를 확인하였다.
2. 실험 셋 업
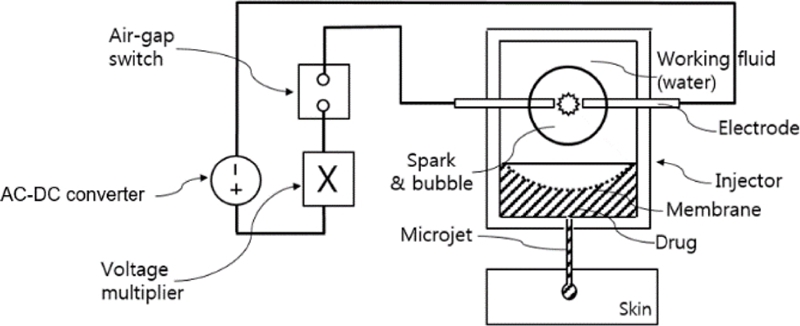
Fig. 1과 같이 마이크로젯 약물 주입 장치는, 밀폐된 내부 공간에 작동 유체가 채워진 압력 챔버와 내부에 약물 용액이 수용되며 마이크로 노즐이 형성된 약물 챔버와 확장 및 원상 회복이 가능하도록 탄성을 가지는 막으로 압력 챔버와 약물 챔버의 사이를 분리 구획하는 탄성막 및 압력 챔버 내의 작동 유체에 에너지를 집중시켜 버블을 발생시키는 에너지 집중 장치(레이저, 절연파괴)를 포함하며 또한, 약물 챔버와 연결되어 약물 공급로를 통해 내부에 저장된 약물 용액을 약물 챔버로 공급하는 약물 저장고로 구성된다. Fig. 2는 이를 구현한 레이저 핸드피스, 전기식 절연 파괴 핸드피스의 모습이다.
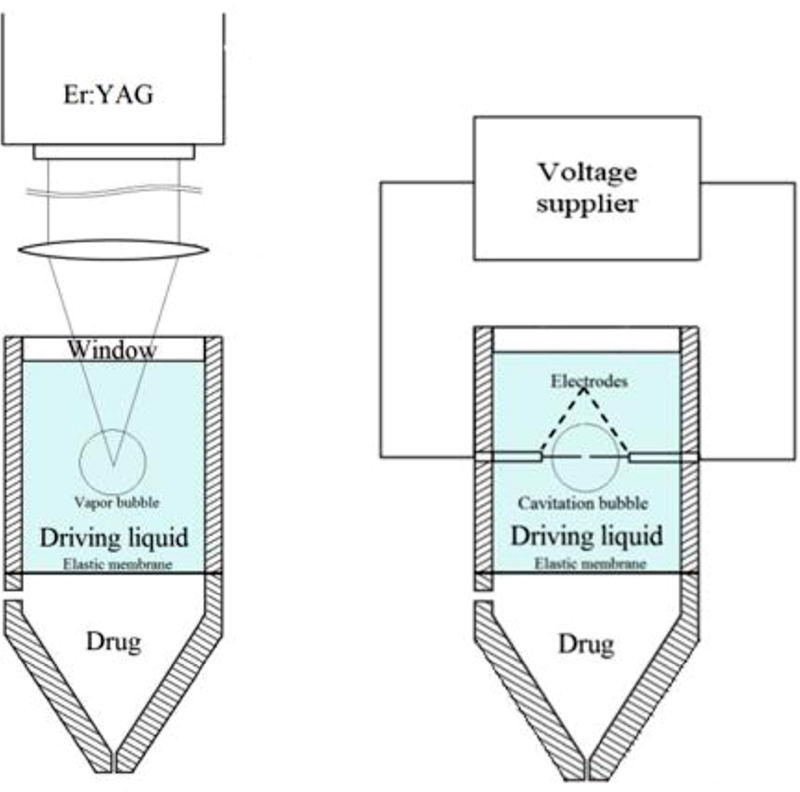
Schematic of a underwater spark discharging power sources and drug chamber nozzles attached to a pressure chamber
2.1 파워 소스
마이크로젯 인젝터에 있어 약물 용액을 마이크로젯을 분사 추진시키는 원동력은 압력 챔버에 채워진 작동 유체로부터 발생하는 것이다. 작동 유체의 4 mm2에 해당하는 미소 면적에 1-2 J의 에너지를 가하면 작동 유체가 순식간에 증발하여 증기 버블이 발생하며 팽창하게 된다. 이는 본 연구에서 다루는 약물 전달 장치의 구동력이 된다. 레이저 에너지를 제공하기 위해 Er:YAG를 사용하였으며 150 μs의 펄스 지속 시간과 2.940 μm의 파장을 갖는다. 펄스 주기는 10 Hz며 모든 실험에서 레이저플루언스(Laser Fluence)는 모든 실험에서 87 J/cm²이다.
또한 초점 길이가 100 mm인 볼록 렌즈를 통하여 레이저 빔을 압력 챔버에 대하여 집중시켰다. 작동 유체로써 물은 2.950 μm의 파장에서 가장 높은 흡수계수(약 15000 cm-1)를 갖기 때문에 레이저 에너지에서 역학에너지로의 높은 변환 효율에 Er:YAG 레이저가 적합하다.13 미소 면적에 레이저를 집중시킬 경우 발생하는 버블은 증기 버블이며 이는 약 280 μs 동안 팽창하여 해당 시간 동안 구동력을 제공한다.6 하지만 레이저 에너지는 전기에너지에서 복사에너지, 열에너지, 운동에너지로 변환되는 여러과정을 거치기 때문에 에너지 효율이 비교적 낮으며 따라서 전체 장비의 크기가 크다. 절연파괴에 의한 에너지는 전기 에너지에서 운동에너지 형태로 바로 변환하기 때문에 비교적 높은 효율을 갖는다. 파워서플라이에서는 캐패시터 모듈에 충분한 전위차를 주고 전위량을 일정시간 동안 충전한다. 일정 전위량이 충전되면 이를 인젝터의 압력 챔버 내 구동액에 방출하여 스파크를 일으키게 된다. 이러한 스파크로 인해 압력 챔버의 일정 영역에 케비테이션 버블이 생성된다. 케비테이션 버블은 구동액에 특정 전압 이상이 인가될 때 구동액이 절연파괴되어 순식간에 구동액이 플라즈마로 상변화하는 과정이다.14,15
따라서 절연파괴에 이용하면 전기에너지를 바로 운동에너지로 변환할 수 있는 장점이 있다. 케비테이션 버블이 순식간적으로 팽창함에 따라 인젝터 노즐의 약물을 밀어내게 되며 이러한 과정을 초당 10회 반복한다.
작동 유체 내에 생성된 버블은 순간적으로 팽창하였다가 에너지 인가를 중지하면 소멸하는데, 이러한 버블의 급격한 팽창에 의해 탄성막이 바깥쪽(즉 약물 챔버 방향)으로 신장 변형하게 되고 이러한 탄성막의 변형은 인접한 약물 챔버 내의 약물용액에 압력파를 전달한다. 약물 챔버의 하단부에는 미세 직경의 마이크로 노즐이 형성되어 있어 압력 챔버의 작동 유체가 탄성막을 밀어내는 추진력에 의해 약물 용액이 마이크로 노즐을 통해 고속 마이크로젯 분사될 수 있도록 구성된다.
절연파괴에 의한 에너지는 Fig. 3에 나타낸 시스템에 의해 제공된다. 이는 220 V 입력 AC-DC 컨버터와 전압 증배기(Voltage Multiplier), 자동 스위치(Auto Switch)에 의해 구성된다. 승압기는 인버터 회로(Inverter Circuit), 변압기(Transformer), 코크로프트-월턴 회로(Cockcroft-Walton Generator Circuit) 와 캐패시터뱅크(Capacitor Bank)로 구성된다. AC-DC 컨버터에서 출력되는 24 DCV 전압은 인버터 회로를 통해 펄스 형태의 전압으로 변환되며 이후 승압기를 통해 200-300 V로 승압된다. 그리고 이는 코크로프트-월턴 회로에 의해 3 kV로 2차 승압되며 캐패시터 뱅크를 충전시킨다. 캐패시터 뱅크의 용량은 1.8 μF이며 이에 해당하는 용량이 충전될 때 자동 스위치가 열리며 0.81 J의 에너지가 전극을 통해 방출되면서 Fig. 1의 압력 챔버 내에 스파크를 유도한다. 모든 에너지가 방출된 이후 자동 스위치는 닫히고 캐패시터 뱅크가 충전되며 동일한 과정이 7 Hz의 주기로 반복된다. 전극의 재료는 스테인레스스틸(Stainless Steel)이며 길이 12 mm, 직경 1 mm의 핀 형상을 갖는다.
2.2 비디오 이미징
본 연구에서 인젝터의 성능이 약물 분사 횟수에 상관없이 동일함을 입증할 수 있는 기준 중의 하나는 약물의 분사 속도이다. 약물의 분사 속도는 초고속 카메라(Phantom v711)를 이용하여 42,011 fps의 촬영 속도와 1280 × 800의 분해능을 가지고 촬영되었다. 촬영된 이미지의 초점 거리에서 픽셀당 실제 측정 간격을 계산하고 카메라 어플리케이션인 PCC 2.7을 이용하여 속도를 측정하였다. 젯 속도는 노즐 끝단을 기준으로 측정하였다.
2.3 약물 전달 여부 평가
약물 전달 성능을 입증할 수 있는 기준으로 돼지 피부 조직을 대상으로 하는 침투 깊이를 측정하였다. 돼지피부의 경우 10-30 Mpa의 항복인장 강도를 가지며 사람의 피부의 항복인장강도는 2-15 Mpa로 본 연구 결과로부터 인체를 대상으로 한 경우의 결과를 예상해 볼 수 있다.16 FFPE (Formalin-Fixed, Paraffin-Embedded) 기법으로 약물이 침투된 조직의 단면을 가시화했으며 또 이를 H&E (Hematoxylin & Eosin) Stain 기법으로 염색한 후 전과 같은 FFPE 기법을 통하여 단면을 광학현미경으로 촬영한 결과를 얻을 수 있다. 이를 통해 약물이 조직으로 침투된 결과를 가시화 할 수 있다.
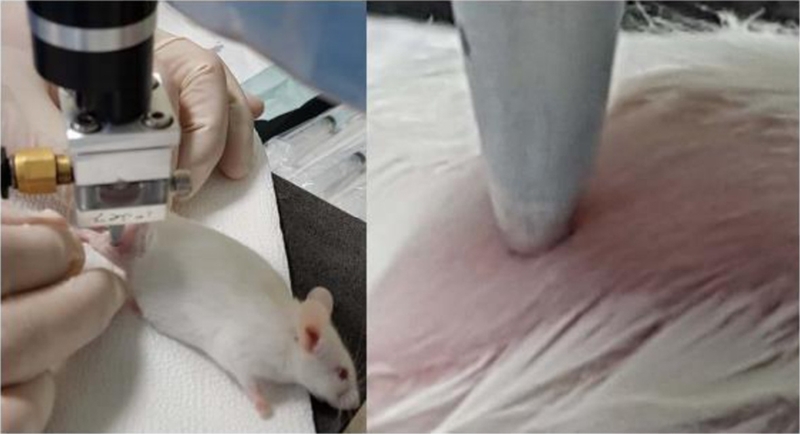
또한 약물이 침투된 조직에서 체내에 흡수되어 효능을 발생시키는지 여부를 확인할 수 있다. 이는 제 1형 당뇨 마우스 모델에 인슐린을 주입하고 이에 따른 혈당 변화를 통해 확인 할 수 있다. 마우스 모델 수컷 15마리를 사육하였다. 당뇨 유발 물질을 조제하기 위하여 Steptozotocin 400 mg을 사용하였고 5°C에서 보관하였다. 투여 당일 용매에 Steptozotocin을 25 mg/ml로 용해하여 조제하였다. 이를 복강 투여하여 당뇨 질병을 유발시켰다. 약물 전달 평가를 위해 사용한 물질은 인슐린(휴물린R주)이며 100 IU/ml이다. 이를 생리 식염수에 1 : 1 비율로 희석하여 주사기(30 G) 및 마이크로젯 인젝터를 사용하여 마우스 한 마리당 100 μL를 피하로 투여하였다. Fig. 4는 이러한 당뇨 마우스 실험 시 인슐린 투여 모습이다. 주사기를 이용한 투여 시간은 한 마리당 각 약 5초이며 마이크로젯 인젝터를 이용한 투여시간은 한 마리당 약 20초이다.
3. 실험 결과
3.1 파워 소스에 따른 젯 성능
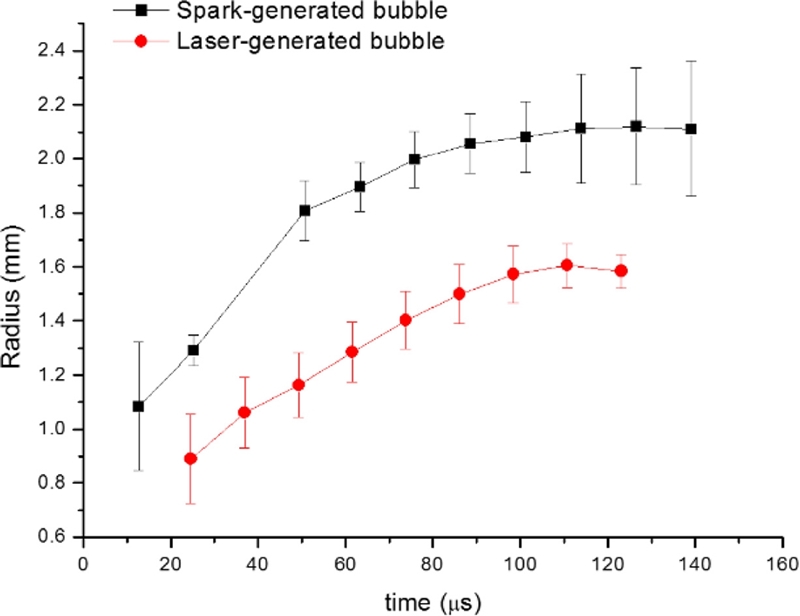
Fig. 5는 절연파괴에 의한 케비테이션 버블을 초고속으로 촬영한 것이다. 케비테이션 버블은 113 μs까지 팽창하며 최대 부피 28.26 mm3에 도달한다. 따라서 팽창 속도는 250.0 mm3/ms이다. Fig. 6은 각 파워 소스에 따른 버블의 팽창 과정을 시간에 따른 버블 직경으로 나타낸 것이다. 해당 절연파괴에 의한 버블의 팽창 속도는 레이저에 의한 버블 팽창속도의 3.3배이다. 이를 통해 레이저 에너지에 비해 전기식 절연 파괴 에너지로 인해 더욱 빠른 버블 팽창 속도를 얻을 수 있음을 알 수 있다. 버블의 팽창 속도는 약물 분사 속도에 비례하며 따라서 전기식 절연 파괴에 의해 더 빠른 마이크로젯 속도 및 침투 성능을 얻을 수 있다. Fig. 7은 절연파괴 에너지를 적용하여 생성한 마이크로젯의 분사 과정을 촬영한 것이다. 이러한 버블 팽창이 실제 마이크로젯 분출의 구동력이 될 수 있음을 나타내고 있으며 이는 버블이 팽창함에 따라 탄성막을 밀어내고 노즐의 약물을 분사하는 과정을 촬영한 것이다.
3.2 입력 신호 조절에 따른 젯 성능 제어
Fig. 8은 압력 챔버 전극에 인가되는 전류값을 조절하여 약물이 분사되는 주기를 조절한 것이다. 입력되는 전류는 I = 1/2 CVf로 표현할 수 있으며 이때 C는 커패시터용량이며 V는 전압, f는 약물 분사 주기이다. 일정한 입력전류에서 전극에 가해지는 전압이 증가할수록 일정한 분사주기를 가지기 위한 인가 전류값은 증가한다.
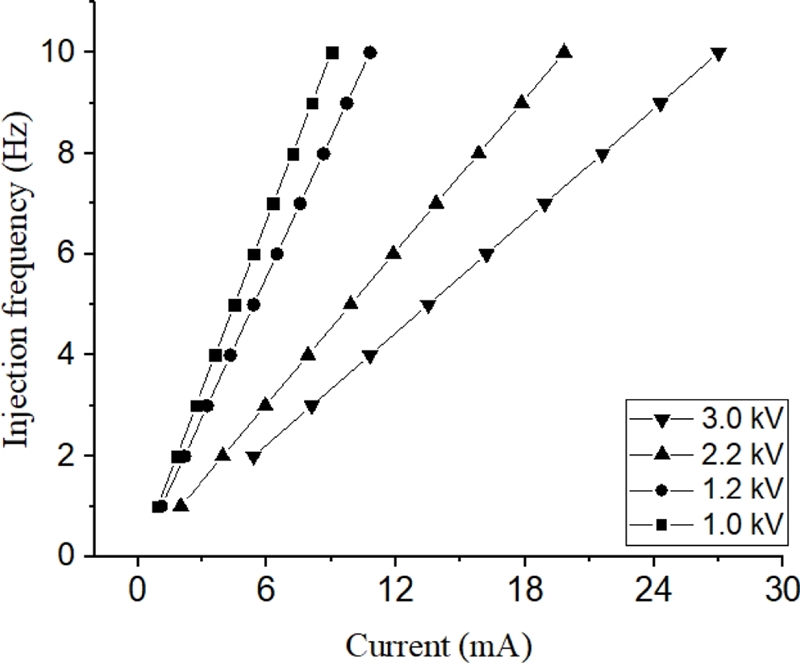
Changes in the injection frequency with input current. Each case of experiment was performed 5 times
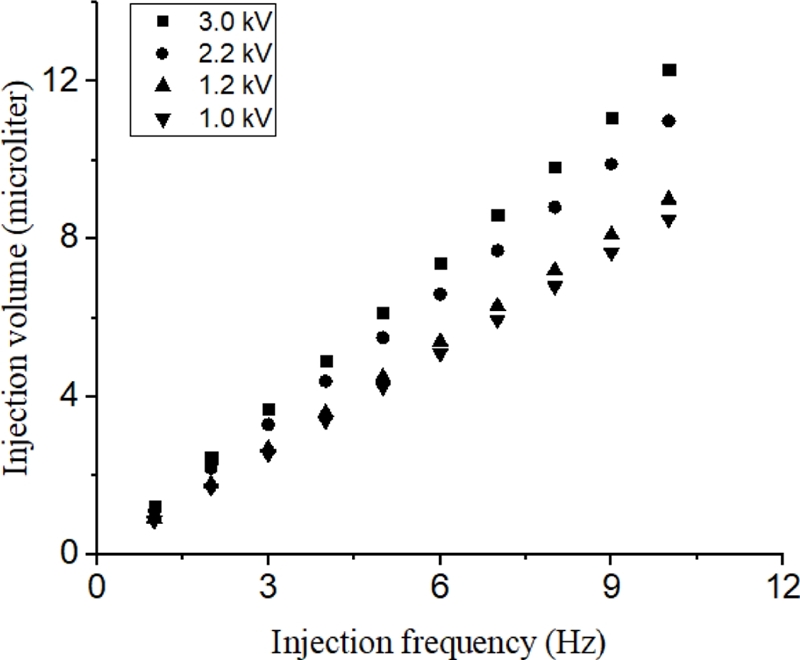
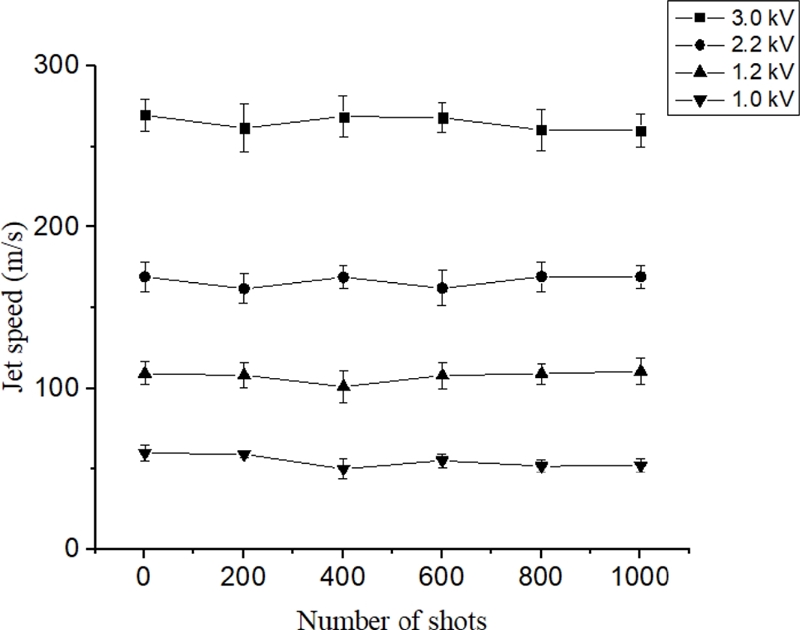
Fig. 9는 약물 분사 주기를 조절함에 따라 변화하는 약물 분사량이다. 이 때 약물 분사량은 각 분사주기에 따른 1초당 분사량이며 분사주기가 1-10 Hz까지 증가함에 따라 분사량 또한 비례하여 초당 0.85-1.23 μl까지 변화한다. Fig. 10은 인가 전압에 따른 약물 주입기의 젯속도를 나타낸 것이다. 입력 전압이 증가함에 따라 발생하는 케비테이션 버블의 팽창 속도가 증가하며 이에 의해 약물이 방출되는 젯속도가 증가한다. 하지만 Fig. 8에서 설명한 바와 같이 인가 전압이 증가할수록 일정한 약물 분사주기를 가지기 위하여 필요한 커패시터 충전에너지가 증가하며 그러므로 입력 전류값이 증가한다.
3.3 침투 실험
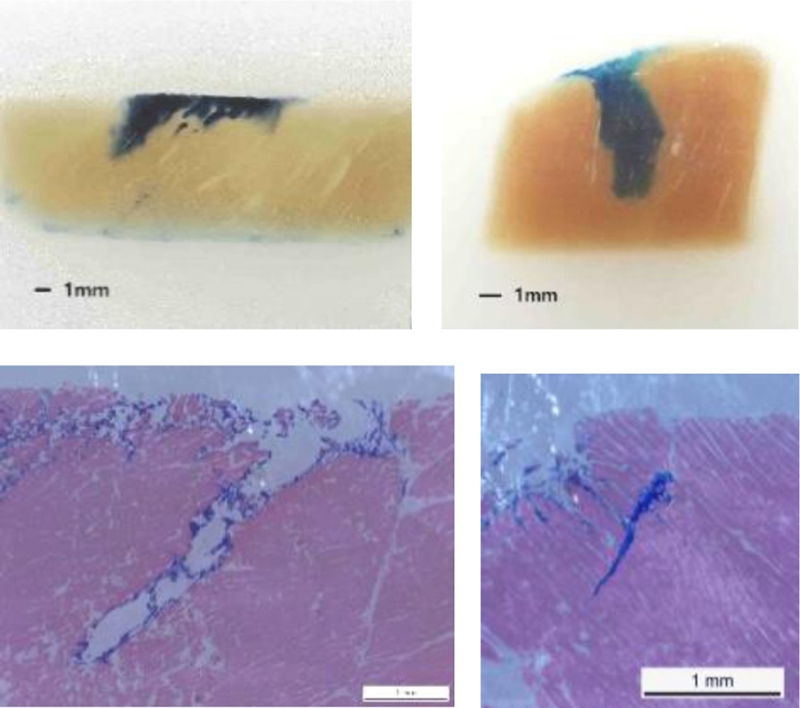
Fig. 11은 Chlorhexidine 수용액을 돼지 등심 조직에 주입한 것이다. 위 그림은 FFPE 기법을 이용하여 조직을 block 형태로 보관하여 슬라이스 처리를 한 것이며 아래는 H&E (Hematoxylin & Eosin) Dye를 통해 조직을 염색하여 FFPE 기법을 이용하여 조직을 block 형태로 보관하여 슬라이스 처리를 한 것이다. 침투 깊이는 약 3-5 mm이며 조직의 결에 관계없이 조직을 뚫고 침투 되었음을 나타낸다. 이는 피부 진피층에 약물이 전달 된 것이라 할 수 있다.
3.4 당뇨병 마우스모델을 이용한 인슐린 주입 효능 시험
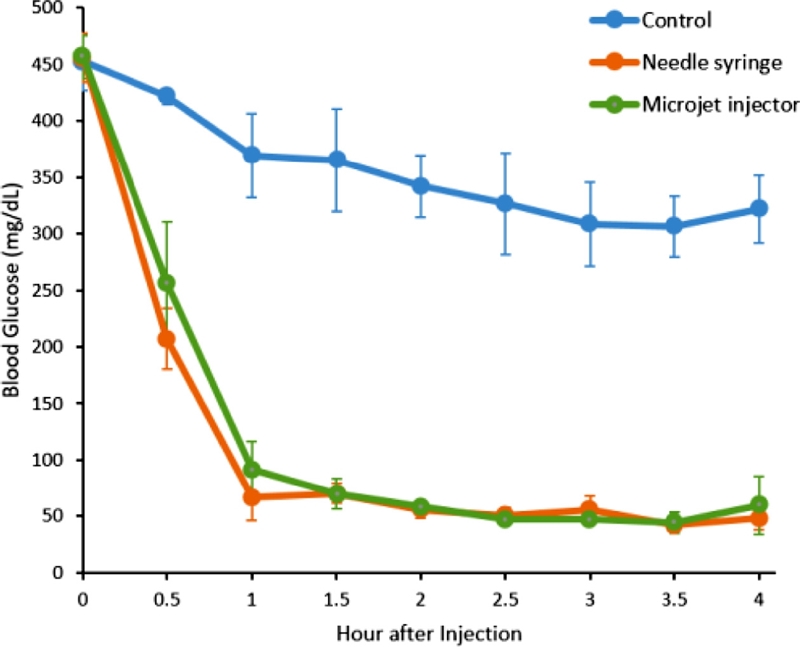
인슐린 의존성 제 1형 당뇨 마우스모델을 이용하여 마이크로젯 인젝터의 혈당 조절에 대한 효능을 평가하였다. 기존의 바늘형 주사기와 동일한 방법으로 인슐린을 투여하여 생체 내에서 혈당의 변화를 비교하였다. 수컷의 마우스에 Streptozotocin을 1회 투여하여 당뇨병을 유발시킨 후 3일이 경과된 다음, 각 마우스의 꼬리 정맥으로부터 미량의 혈액을 채취하여 혈당을 측정하였다. 이 때 비교군 마우스 5마리의 평균 혈당은 452.4 mg/dL이었다. 인슐린 투여 후 바늘형 주사기 시험군 5마리의 평균 혈당은 456.2 mg/dL, 마이크로젯 인젝터 시험군 5마리의 평균 혈당은 456.8 mg/dL였다. Fig. 12와 같이 마이크로젯 인젝터로 인슐린이 투여된 시험군에서 투여 후 30분 이후부터 효과적으로 혈당이 저하되었으며, 1시간 경과 이후부터 총 4시간의 시험시간동아 낮은 혈당을 지속적으로 유지하였다. 이는 대조군과 비교하여 통계적으로 유의성 있는 효과를 나타낸 것이며, 또한 기존의 인슐린 주사기 방법과 비교하여 동일한 혈당 변화의 결과를 나타낸다. 질병 유발 및 인슐린 투여기간 동안 비정상적인 임상소견은 발견되지 않았으며 시험 물질 또는 투여 장비에 따른 특이적 독성은 나타나지 않았다.
4. 결론
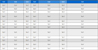
Table 1은 본 연구에서 개발한 무바늘 약물 전달 시스템과 타사 제품 또는 선행 연구 개발된 약물 전달 시스템의 약물 주입량과 해당하는 주입 시간을 나타낸 것이다. 타 시스템의 경우 약물 0.12-0.15 ml를 주입하는데 걸리는 시간은 0.01-0.1초 이내이며 ‘Intraject’의 경우 0.5 ml를 주입하는데 0.06초가 소요된다.17,18 0.12-0.5 ml에 해당하는 약물로써 호르몬제 등이 사용되며 이러한 양이 비교적 빠른 시간 내에 인체에 전달된다. 본 연구에서 개발된 시스템은 Fig. 8에서 나타낸 바와 같이 0.12 ml의 약물을 10초에 걸쳐 전달한다. 이는 타 시스템에 비해 비교적 소량의 양을 넓은 시간 범위에 전달하는 것이며 많은 양의 약물은 짧은 시간에 주입할 경우 발생할 수 있는 조직의 파열과 통증을 저감하기 위한 것이다.
이전부터 감염, 자원 낭비 등의 침습식 주사의 단점을 해결하기 위하여 미세 직경을 가지는 마이크로젯 형태의 약물을 비침습적으로 분사하는 마이크로젯 약물 전달 시스템이 개발되었다. 이러한 약물 전달 시스템을 레이저 및 전기식 절연 파괴 파워소스를 이용하여 구현 하였다. 전기식 절연 파괴 파워소스를 사용할 경우 레이저와는 달리 에너지 변환 과정이 적기 때문에 효율이 좋다는 장점이 있다. 따라서 본 연구에서는 약물 전달 장치의 구동력으로써 전기식 절연 파괴를 채택하는 바이다. 이러한 약물 전달 시스템은 액체 내 절연파괴를 구동력으로써 이용하여 약물을 분사하는 방식을 가지고 있으며 기존 바늘식 주사에 비해 적은 통증을 유발하고 상처 없이 약물을 투입할 수 있다. 본 연구를 통해 개발된 약물 전달 시스템은 피부의 진피층(Epidermis)을 투과하여 약물을 전달할 수 있는 성능을 가지며 진피층만 침투되어도 효력이 발생하는 단백질 계 호르몬제(Clorhexidine, 인슐린)과 타투 잉크 등의 주입에 적용될 수 있다. 또한 본 연구의 약물 전달 시스템을 통하여 당뇨병이 걸린 마우스모델에 효과적으로 적용하였다. 주입된 인슐린이 혈당 저하효능을 나타내었으며 약물 주입 성능에 있어서 기존 바늘식 주사 방법과 동등한 효능을 나타내는 것으로 판단된다. 이는 많은양의 에너지를 짧은 인터벌에 방출하는 구동력을 이용하였고 분사 횟수에 상관없이 성능을 유지시키는 메커니즘이 적용되었으므로 약물을 넓은 부위에 고르게 주입할 수 있으며 분사 횟수를 조절하여 침투 깊이 및 약물 전달량을 조절할 수 있다. 그러므로 각각 치주 질환, 호르몬치료(당뇨), 피부 미용 등의 분야에 사용되는 기존 기기를 대체할 수 있고 기존의 기기의 난제였던 가동 반복성과 침투 성능을 향상시켜 새로운 의료 분야에도 활용될 것으로 전망된다.
Acknowledgments
이 논문은 2018년도 한화시스템(주)의 재원을 지원 받아 수행된 연구임.
REFERENCES
-
Stachowiak, J. C., von Muhlen, M. G., Li, T. H., Jalilian, L., Parekh, S. H., et al., “Piezoelectric Control of Needle-Free Transdermal Drug Delivery,” Journal of Controlled Release, Vol. 124, Nos. 1-2, Paper No. 88-97, 2007.
[https://doi.org/10.1016/j.jconrel.2007.08.017]

-
Han, T. H. and Yoh, J. J., “A Laser Based Reusable Microjet Injector for Transdermal Drug Delivery,” Journal of Applied Physics Vol. 107, No. 10, Paper No. 103110, 2010.
[https://doi.org/10.1063/1.3430989]

-
Arora, A., Prausnitz, M. R., and Mitragotri, S., “Micro-Scale Devices for Transdermal Drug Delivery,” International Journal of Pharmaceutics, Vol. 364, No. 2, pp. 227-236, 2008.
[https://doi.org/10.1016/j.ijpharm.2008.08.032]

-
Taberner, A., Hogan, N. C., and Hunter, I. W., “Needle-Free Jet Injection Using Real-Time Controlled Linear Lorentz-Force Actuators,” Medical Engineering & Physics, Vol. 34, No. 9 pp. 1228-1235, 2012.
[https://doi.org/10.1016/j.medengphy.2011.12.010]

-
Timoshkin, I., Fouracre, R., Given, M., and MacGregor, S., “Hydrodynamic Modelling of Transient Cavities in Fluids Generated by High Voltage Spark Discharges,” Journal of Physics D: Applied Physics, Vol. 39, No. 22, pp. 4808-4817, 2006.
[https://doi.org/10.1088/0022-3727/39/22/011]

-
Mackersie, J. W., Timoshkin, I. V., and MacGregor, S. J., “Generation of High-Power Ultrasound by Spark Discharges in Water,” IEEE Transactions on Plasma Science, Vol. 33, No. 5, pp. 1715-1724, 2005.
[https://doi.org/10.1109/TPS.2005.856411]

-
Yoh, J. J., Jang, H. J., Park, M. A., Han, T.-H., and Hah, J. M, “A Bio-Ballistic Micro-Jet for Drug Injection into Animal Skin Using a Nd:Yag Laser,” Shock Waves, Vol. 26, No. 1, pp. 39-43, 2016.
[https://doi.org/10.1007/s00193-015-0565-4]

-
Park, M. A., Jang, H. J., Sirotkin, F. V., and Yoh, J. J., “Er:Yag Laser Pulse for Small-Dose Splashback-Free Microjet Transdermal Drug Delivery,” Optics Letters, Vol. 37, No. 18, pp. 3894-3896, 2012.
[https://doi.org/10.1364/OL.37.003894]

-
Jang, H. J., Hur, E. G., Kim, Y. K., Lee, S. H., Kang, N. G., et al., “Laser-Induced Microjet Injection into Preablated Skin for More Effective Transdermal Drug Delivery,” Journal of the Biomedical Optics, Vol. 19, No. 11, Paper No. 118002, 2014.
[https://doi.org/10.1117/1.JBO.19.11.118002]

-
Han, T. H, Hah, J. M. and Yoh, J. J., “Drug Injection into Fat Tissue with a Laser Based Microjet Injector,” Journal of the Applied Physics, Vol. 109, No. 9, Paper No. 093105, 2011.
[https://doi.org/10.1063/1.3584813]

-
Ham, H. C., Jang, H. J., and Yoh, J. J., “A Check Valve Controlled Laser-Induced Microjet for Uniform Transdermal Drug Delivery,” AIP Advances Vol. 7, No. 12, Paper No. 125206, 2017.
[https://doi.org/10.1063/1.4999962]

- Brennen, C. E., “Cavitation and Bubble Dynamics,” Oxford University, 1995.
-
George, M. H. and Marvin, R. Q., “Optical Constants of Water in the 200-nm to 200-μm Wavelength Region,” Applied Optics, Vol. 12, No. 3, pp. 555-563, 1973.
[https://doi.org/10.1364/AO.12.000555]

-
Hontañón, E., Palomares, J. M., Stein, M., Guo, X., Engeln, R., et al., “The Transition from Spark to Arc Discharge and Its Implications with Respect to Nanoparticle Production,” Journal of Nanoparticle Research, Vol. 15, Paper No. 1957, 2013.
[https://doi.org/10.1007/s11051-013-1957-y]

-
Vokurka, K. and Plocek, J., “Experimental Study of the Thermal Behavior of Spark Generated Bubbles in Water,” Experimental Thermal and Fluid Science, Vol. 51, pp. 84-93, 2013.
[https://doi.org/10.1016/j.expthermflusci.2013.07.004]

-
Khatam, H., Liu, Q., and Krishnaswa, R. C., “Dynamic Tensile Characterization of Pig Skin,” Acta Mechanica Sinica, Vol, 30, No. 2, pp. 125-132, 2014.
[https://doi.org/10.1007/s10409-014-0042-9]

-
Schoubben, A., Cavicchi, A., Barberini, L., Faraon, A., Berti, M., et al., “Dynamic Behavior of a Spring-Powered Micronozzle Needle-Free Injector,” International Journal of Pharmaceutics, Vol. 491, Nos. 1-2, pp. 91-98, 2015.
[https://doi.org/10.1016/j.ijpharm.2015.05.067]

- Chavan, B., Doshi, A., Malode, Y., and Misal, B., et al., “Review on Needle Free Drug Delivery Systems,” International Journal of Pharma Research & Review, Vol. 2, No. 9, pp. 30-36, 2013

Ph.D. Candidate in the Department of Mechanical & Aerospace Engineering, Seoul National University. His research interest is underwater spark discharge and pulsed flow.
E-mail: hamn2012@snu.ac.kr

Doctoral Research Staff in the Department of Mechanical & Aerospace Engineering, Seoul National University. His research interest includes underwater spark discharge and microjet injection system.
E-mail: therin21@snu.ac.kr

Senior Engineer in Hanwha Systems. His research interest is future combat systems.
E-mail: yg1021.kim@hanwha.com

Professor in the Department of Mechanical & Aerospace Engineering, Seoul National University. His research interest includes physics of matters at extreme states.
E-mail: jjyoh@snu.ac.kr