요추용 자립형 추간체 유합 보형재의 MRI 코일 내 무선주파수 및 동물시험을 통한 발열성 평가
1오송첨단의료산업진흥재단 첨단의료기기개발지원센터Copyright © The Korean Society for Precision Engineering
This is an Open-Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
Most of passive implants belong to medical device are consist of metallic and nonmetallic materials. According to the sort of components, it makes more influence into the human body. In this study, we performed induced-RF (Induced-Radio Frequency) heating evaluation which is part of MRI (Magnetic Resonance Imaging) compatibility and safety test and in-vivo pyrogen test with lumbar stand-alone cage. RF from 3T MRI coil was radiated on medical device, and provided heat nearby stand-alone cage. Thermal change detected areas are distinguished by metallic and nonmetallic part. As followed detection areas, febrility was shown and metallic part was slightly higher than control area, nonmetallic part. Furthermore, stand-alone cage was performed in accordance with in-vivo pyrogen test, and solution injected rabbits had no fever for test period. Through physically and biologically evaluated stand-alone cage, exothemic reaction was observed and we predicted the effect when it would be inserted in patient.
Keywords:
Stand-alone cage, Magnetic resonance imaging compatibility and safety, Induced-radio frequency heating evaluation, Pyrogen test키워드:
자립형 추간체 유합 보형재, MRI 적합안전성, 무선주파수 유도 발열성 평가, 발열성 시험1. 서론
척추 질환의 외과적 치료로 쓰이는 의료기기 중 하나인 자립형 추간체 유합 보형재는 추간제의 높이와 척추의 굴곡을 복원시켜주며, 척추체를 구조적으로 지지하여 척추의 생체역학적 안전성을 복원하는 역할을 한다.1
침습적 시술로 체내에 삽입이 되는 추간체 유합 보형재는 금속 및 비금속 등이 재료로 주로 사용 되고 있다.2 하지만 시술 후 구조 및 설계 등 운동성에 관한 문제들이 대두되고 있으며, 그 외에 생물학적 안전성과 MRI (Magnetic Resonance Imaging) 적합안전성3 등의 문제들이 고려되고 있다.
특히나 이러한 전원공급이 필요 없는 인체 이식형 의료기기는 환자가 실제 MRI 촬영 시 시술 받은 부위에서 국소적인 발열 등을 느낄 수 있으며, MRI를 촬영하기 위해서는 전문의와 상담이 필요하다. 이에 대해 FDA (Food and Drug Administration)에서는 MRI 촬영 시 발열, 이동, 이미지 왜곡에 대한 MRI 적합안전성 시험을 언급하였지만, 전 세계적으로 이 시험을 할 수 있는 기관은 Shellock3을 비롯하여 몇 군데 되지 않는 상황이다.
최근 식품의약품안전처에서는 이러한 의료기기의 MR (Magnetic Resonance) 환경 안전성에 대한 가이드라인이 배포 되었다.4 이미 FDA, CE (Communaute Europeenne) 등 국외 기관에서는 전원 공급이 필요 없는 인체 이식형 의료기기를 수출하는 회사에게 MRI 적합안전성 시험을 요구하고 있으며, 앞으로는 국내 인허가 획득 시 적용될 전망이다.
MRI 적합안전성 시험 중 하나인 무선주파수에 의한 발열성 평가는 MRI 내의 B1 영역으로부터 의료기기에 끼치는 영향을 발열 정도로 평가하는 것으로 환자가 MRI 촬영 시 느끼는 발열과 동일한 현상이다.5
또한 MRI의 발열성 평가는 의료기기 물리적 현상을 관찰하는 시험인 반면, 의료기기의 용출물을 이용하여 생물학적 발열반응을 감지하는 발열성물질시험법이 있다. 이 시험법은 토끼를 시험 개체로 이용하며 대한약전 일반시험법의 발열성물질시험법을 따른다.6
본 연구에서는 자립형 추간체 유합 보형재의 MRI 코일 내의 발열 및 동물을 이용한 발열성 시험을 수행하였다. 3T MRI 코일내에서 자립형 추간체 유합 보형재의 발열 정도를 계측하여, 환자들의 MRI 촬영 시 느낄 수 있는 발열을 예측하였으며, 동물을 이용한 발열성물질시험을 통하여 이 의료기기의 생물학적 안전성을 확인하였다.
2. 시험방법
2.1 재료
본 연구에서 사용된 자립형 추간체 유합 보형재(ALIF Stand-Alone Cage-2846-4818, GS Medical, Osong, Korea)는 몸체(Body), 전방 플레이트(Plate), 스크류(Screw), 잠김 플레이트(Locking Plate) 총 4 개 파트로 구성되어 있다. 몸체에 사용된 재료는 Polyether Ether Ketone (PEEK)이며, 전방 플레이트, 스크류, 잠김 플레이트에 사용된 재료는 티타늄합금인 Ti6Al4V이다.
2.2 시험 장비
온도 계측 위치를 선정하기 위하여 MRI 발열 시뮬레이터(Sim4Life, Zurich Med Tech, Swiss)를 통하여 예비 시험을 하였다. 이후 실제 3T MRI 코일 내부 환경과 동일한 조건으로 시험을 위하여 임플란트 MRI 평가 시스템(MITS 3.0, Zurich Med Tech, Swiss)을 사용하였다. MRI 코일 내 발열을 평가하기 위하여 전자계 온도 계측기(EASY4MRI, SPEAG, Swiss)를 사용하였으며, 발열용 매질(TGe78c0.47@64, Zurich Med Tech, Swiss)와 팬텀(ASTM 2009, Zurich Med Tech, Swiss)를 사용하였다.
발열성물질시험에서 온도를 측정하기 위하여 Digital Thermometer (TMP 812 RS, Panlab SL, Spain) 장비를 사용하였다.
2.3 무선 주파수(Radio Frequency)에 의한 발열 평가
본 시험은 ASTM F21827 규격의 절차에 따라 진행하였다. MRI 발열 시뮬레이터를 통하여 MRI 코일 내 팬텀에서 무선주파수에 가장 영향을 많이 받는 곳을 확인하였다. 이후 매질을 채운 팬텀을 MRI 코일의 정중앙에 배치한 후, 시뮬레이터로 살핀 최고 온도 변화를 지닌 곳과 그곳으로부터 대칭을 이루는 반대편에서 온도를 계측하였다. 추간체 유합 보형재를 최고 온도 변화를 지닌 곳에 설치하여 동일 시험을 반복하여 추간체 유합 보형재가 없을 때와 있을 때의 온도 변화를 평가한다. 모든 시험은 전신 평균 전자파흡수율(Whole Body Averaged SAR (Specific Absorption Rate))이 2 W/kg 이상이 되는 환경에서 시험하였다.
2.4 발열성물질시험법
대한약전에 의거하여 시험하였으며, 동물시험은 오송첨단의료 산업진흥재단 IACUC 실험동물운영위원회 승인을 받아 진행하였다. 시험동물은 New Zealand White계 2 kg 이상의 수컷 토끼(Male, 2 - 2.5 kg, OrientBio Inc, Seongnam, Korea)를 사용하였고, 시험 전 2일간 이내에 주사를 제외한 전 조작이 포함된 플라시보 시험을 하여 시험 환경에 적응시켰다. 시험액은 생리식염수를 용매로 사용하여 37°C에서 24시간 동안 교반시켜 용출하였다. 시험용량은 체중 kg 당 검액 10 ml로 주사하였고, 시험동물이 안정되었을 때 체온을 계측하여 대조체온으로 설정하고 30분 이내에 검액을 주사하였다. 검액을 주사 할 시험동물 간 대조체온의 차이는 1°C 이하인 상태 및 각 개체별 대조체온의 값이 39.8°C 미만인 상태에서 진행하였다. 검액은(37 ± 2)°C로 가온하여 이정맥에 주사하였고, 시험동물 당 투여 시간은 10분 이내로 하였다. 최종 투여 후 체온은 30 분 간격으로 6 회 측정하였다.
3. 결과
3.1 무선주파수에 의한 발열 결과 분석
팬텀 내 시험 재료의 위치를 선정하기 위하여 MRI 발열 시뮬레이터를 통하여 MRI 코일 내 팬텀에서 무선주파수에 의해 가장 영향을 많이 받는 곳을 선정하였다. 3T 코일, 팬텀 및 발열용 매질은 실제 시험과 동일 조건으로 설정하였다.
Fig. 1의 시뮬레이션 결과 팬텀 중앙의 좌우 대칭을 이루는 곳에서 무선주파수에 의한 영향을 가장 많이 받으며, 실제 시험 시 시뮬레이션 결과를 반영하였다. Fig. 2와 같이 팬텀 중앙의 좌우 대칭점을 기준으로 한 곳에는 시험용 온도, 다른 한 곳에는 대조용 온도 계측을 하였다.
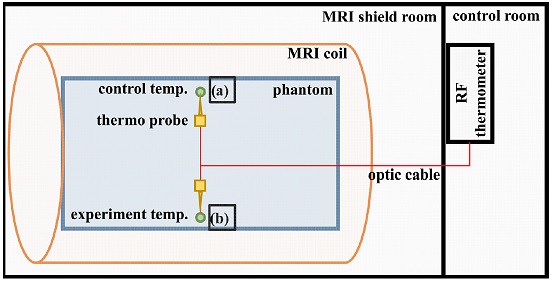
MRI system with MR coil in MRI shield room and control room, Measurement point of (a) control temperature, (b) experiment temperature
실제 MRI 코일의 무선주파수에 의한 시험은 Fig. 2와 같이 전자계 온도 계측기를 측정해야 하는 위치에 맞게 고정하였다. 계측기는 측정해야 하는 지점을 변경할 때마다 다시 고정하였다. 준비가 완료된 팬텀, 계측기는 MRI 코일의 등각점에 팬텀의 중심을 맞춰 놓고, ASTM 팬텀에 발열용 매질을 채운 후 매질 내부의 온도와 MRI 차폐실의 온도가 유사한 상태로 시험을 진행하였다. 무선주파수에 의한 시험은 MRI 차폐실 내에서 진행되며, 온도 계측은 조정실에서 실시간으로 이루어졌다.
Fig. 2의 시험용 온도를 계측하는 곳에서는 총 3가지 조건으로 시험하였다. 추간체 유합 보형재가 없는 상태에서의 발열 정도, 추간체 유합 보형재가 삽입된 상태에서 금속부분의 발열 정도, 추간체 유합 보형재가 삽입된 상태에서 비금속 부분의 발열 정도로 구분하였다.
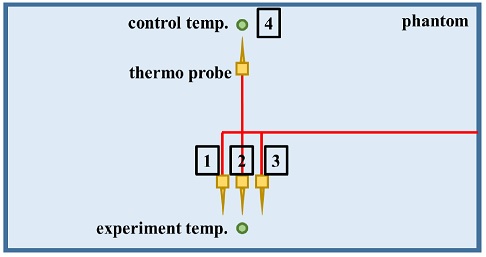
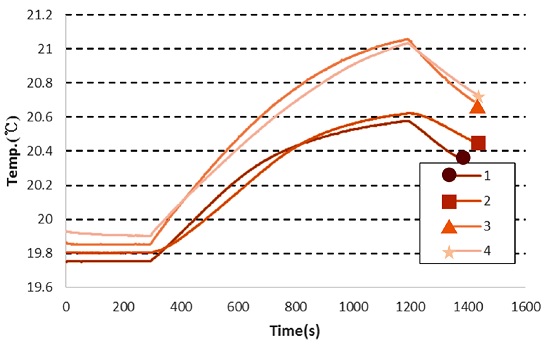
추간체 유합 보형재가 없는 상태로 Fig. 3에서 보이는 1 - 4의 지점에서 온도를 계측하였다. RF 발열 시뮬레이터를 통해 시험용 온도를 계측하는 곳인 2에 한 지점, 그 지점을 기준으로 좌우 1 cm 거리에 있는 곳인 1, 3 지점에서 온도를 계측하였다. 또한 대조용 온도를 계측하는 곳인 4에서 한 지점 총 4 개의 지점에서 온도를 계측하였다.
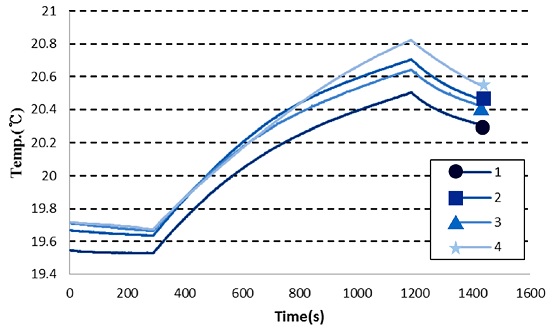
Fig. 4는 MRI 코일 내 추간체 유합 보형재가 없는 상태로 15분간 무선주파수를 조사했을 때의 온도 변화 그래프이다. 무선주파수를 조사하기 전후로 5분 간격을 두어 온도 변화에 대한 안정화 및 무선주파수 조사 완료에 대해 확인하였다. Table 1을 통하여 (b) 구역의 1 - 3 번과 (a) 구역의 4 번 온도를 비교하였다. 2번과 4 번이 팬텀 중간의 대칭을 이루며, 1, 3 번은 2 번 위치에서 각 1 cm 간격을 두었을 때의 온도 변화를 나타낸다. 1 - 3 번 평균온도 변화는 1.01°C로 4번의 온도차인 1.15°C과 비교하여 -0.14°C차이가 난다. 실제 MRI 코일 내의 시험과 동일한 조건을 가지는 시뮬레이션에서 팬텀의 중앙의 양 쪽 지점은 동일한 온도변화를 보였음에도 불구하고, 실제 시험에서는 (b) 구역보다 (a) 구역에서 더 높은 온도 변화가 있는 것을 확인하였다.
추간체 유합 보형재가 없는 상태의 시험을 통하여 MRI 코일에서 팬텀의 온도 변화를 확인 한 후 추간체 유합 보형재를 팬텀 내(b) 구역에 고정시킨 후 동일 조건에서 시험을 다시 진행하였다.
시험은 추간체 유합 보형재 위치를 고정시킨 상태로 온도 계측기의 탐침을 금속 부분인 ① - ③ 지점, 비금속 부분인 ④ - ⑥ 지점에 고정시켜 나누어 측정하였다. 금속과 비금속에 대한 온도를 측정할 때 대조 온도 또한 함께 측정하였다.
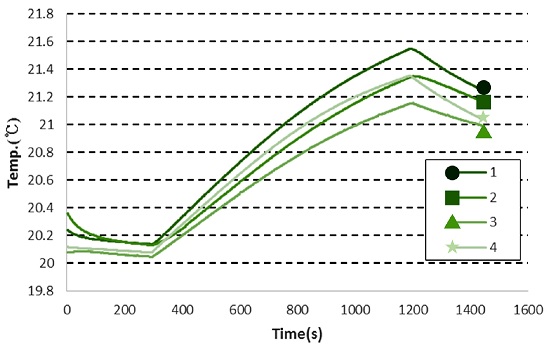
Fig. 6은 추간체 유합 보형재의 금속부분에 해당하는 곳의 온도 결과이다. 추간체 유합 보형재가 없을 때와 동일한 조건이며, Table 2를 통하여 (a) 구역과 (b) 구역의 온도를 비교하였다. (b) 구역은 금속 부분에 해당하며, (a) 구역은 (b) 구역의 온도를 비교하기 위하여 대조 온도를 측정한 지점이다. (b) 구역의 ① ~③ 번은 평균 온도 변화 1.25°C를 보였으며, 이는 (a) 구역과 비교하여 -0.03°C의 온도 차이를 보였다. 추간체 유합 보형재가 없었을 때와 비교하면 추간체 유합 보형재가 있는 상태의 금속 부분의 온도변화가 더 높은 것을 알 수 있다.
Fig. 7은 추간체 유합 보형재의 비금속부분에 해당하는 곳의 온도 결과이다. Figs. 4와 6, 동일 조건이며, Table 3을 통하여 (a), (b)의 온도를 비교하였다. (b) 구역은 비금속 부분에 해당하며, (a)구역은 (b) 구역의 온도를 비교하기 위하여 대조 온도를 측정한 지점이다. (b) 구역의 ④ -⑥ 번은 평균 온도 변화 0.95°C를 보였으며, 이는 (a) 구역과 비교하여 -0.18°C의 온도 차이를 보였다. 추간체 유합 보형재가 없었을 때와 비교하면 추간체 유합 보형재가 있는 상태의 비금속 부분의 온도 변화가 유사한 것을 알 수 있다. 또한 금속 부분에서 온도 변화를 비교하면 금속 부분의 온도 변화 정도가 비금속 부분과 비교하여 높은 것을 알 수 있다.
3.2 발열성물질시험에 대한 결과 분석
대조체온과 투여 후 체온측정치 6회 분을 각각 비교하여, 최대 체온차를 기록하였다. 시험은 시험동물 중 1수라도 0.5°C 이상의 체온상승이 없을 경우 적합으로 판정한다. 시험기간 중 Table 4와 같이 규격에 적합한 무게를 가진 동물을 사용하였으며, 시험 후 사망동물 발견되지 않았다.
Table 5와 같이 대조체온 측정시 개체 간 체온차는 1, 2 번이 0.3°C, 2, 3 번이 0.6°C, 1, 3 번이 0.3°C이며, 각 개체별 체온은 전부 39.8°C 미만으로 규격에 적합한 대조체온을 측정하였다. 투여 후 30 분 간격으로 총 6 회의 체온을 측정하였으며, 모든 개체는 0.5°C 이상의 체온상승을 보이지 않았다. 따라서 본 시험조건 하에서 토끼의 발열반응은 나타나지 않았으므로 시험에 사용된 물질은 발열성이 없으며, 적합한 것으로 사료된다.
4. 결론
본 연구에서는 추간체 유합 보형재에 대한 MRI적합안전성 시험 및 발열성 시험의 일부를 수행하였다. MRI 코일 내에서 시편 금속 부분의 평균 온도 변화가 1.25°C, 비금속 부분에서 0.95°C의 발열을 보였다. 이를 통해 무선주파수의 영향력이 비금속 부분보다 금속 부분에서 더 많은 것을 알 수 있었다. 또한 발열성물질시험을 통하여 각 개체의 적합한 대조체온을 설정하였고, 시편의 용출물에 의한 온도 변화 관찰을 통해 발열 반응이 나타나지 않았음을 확인하였다.
Acknowledgments
이 논문은 2013년도 보건복지부의 재원으로첨단의료산업진흥재단의 지원을 받아 수행한 첨단의료복합단지 연구개발지원사업임(HO13C0004).
REFERENCES
-
Gerber, M., Crawford, N. R., Chamberlain, R. H., Fifield, M. S., LeHuec, J.-C., et al., “Biomechanical Assessment of Anterior Lumbar Interbody Fusion with an Anterior Lumbosacral Fixation Screw-Plate: Comparison to Stand-Alone Anterior Lumbar Interbody Fusion and Anterior Lumbar Interbody Fusion with Pedicle Screws in an Unstable Human Cadaver Model,” Spine, Vol. 31, No. 7, pp. 762-768, 2006.
[https://doi.org/10.1097/01.brs.0000206360.83728.d2]

-
Oxland, T. R. and Lund, T., “Biomechanics of Stand-Alone Cages and Cages in Combination with Posterior Fixation: A Literature Review,” European Spine Journal, Vol. 9, No. 1, pp. 095-101, 2000.
[https://doi.org/10.1007/PL00010028]

-
Shellock, F. G. and Spinazzi, A., “Mri Safety Update 2008: Part 1, MRI Contrast Agents and Nephrogenic Systemic Fibrosis,” American Journal of Roentgenology, Vol. 191, No. 4, pp. 1129-1139, 2012.
[https://doi.org/10.2214/AJR.08.1038.1]

- National Institue of Food and Drug Safety Evaluation, Medical Device Evaluation Department, “Safety Guideline about Passive Implant at Magnetic Resonance,” http://www.mfds.go.kr/index.do?x=0&searchkey=title:contents&mid=1161&searchDivision=&searchClass=&searchword=%C0%DA%B1%E2%B0%F8%B8%ED&y=0&searchSubDivision=&pageNo=1&seq=11182&sitecode=2016-10-04&cmd=v, (Accessed 21 APR 2017)
-
Park, S. M., Kamondetdacha, R., and Nyehuis, J. A., “MRI Safety: RF-Induced Heating Near Straight Wires,” IEEE Transactions on Magnetics, Vol. 41, No. 10, pp.4197-4199, 2005.
[https://doi.org/10.1109/TMAG.2005.854803]

- National Institue of Food and Drug Safety Evaluation, Medical Device Evaluation Department, “Pyrogen Test of Medical Device Applied Guideline,” http://www.mfds.go.kr/index.do?x=0&searchkey=title:contents&mid=1161&searchDivision=&searchClass=&searchword=%B9%DF%BF%AD&y=0&searchSubDivision=&pageNo=1&seq=8234&sitecode=2014-08-21&cmd=v, (Accessed 21 APR 2017)
- ASTM F2182, “Standard Test Method for Measurement of Radio Frequency Induced Heating On or Near Passive Implants During Magnetic Resonance Imaging,” 2011.