적층 제조 기술을 이용한 지능형 약물 전달 시스템의 개발
Copyright © The Korean Society for Precision Engineering
This is an Open-Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
A programmable drug delivery system can control the release rate of a drug. It can minimize side effects while maximizing therapeutic effects. In this research, we investigated the feasibility of producing a programmable drug delivery system using 3D printing technology. A capsule with a micro-orifice and a drug-laden hydrogel was designed. The designed system was then fabricated by the printing process using polycaprolactone and hydrogel. The printed drug delivery system was immersed in PBS at 37°C and the number of molecules released was measured thorough colorimetric analysis. The effect of diameter and length of the micro-orifice and concentration of the hydrogel on drug release characteristics was then determined. The initial burst release rate was found to be increased with increasing orifice size. Increasing the length of the orifice linearly delayed the start time of drug release. At length of 600 μm and 1,200 μm, drug release was initiated after 36 h and 72 h for, respectively. When the concentration of hydrogel was increased, drug release rate tended to decrease. These results successfully confirmed that a drug delivery system with controlled release rate and initiation time could be manufactured using 3D printing technology.
Keywords:
Drug delivery system, Controlled release, Hybrid 3D printing키워드:
약물 전달 시스템, 조절 방출, 복합 3D 프린팅1. 서론
약물 전달 시스템(Drug Delivery System, DDS)은 기존 의약품의 부작용 최소화와 치료 효과의 상승 그리고 환자의 편의성 향상을 위하여 개발되고 있다. 이 시스템은 적용 목적에 따라 약물 방출 속도, 지속시간 등 특정 약동학적 성질과 적절한 투약방법을 갖도록 설계된다.1 그 중 이식용 약물 전달 시스템은 삽입된 국소 부위에만 약물이 전달 되도록 디자인 되어있을 뿐만 아니라, 전신 투약법과 비교했을 때 같은 약효를 얻기 위해 필요한 약물의 양이 적기 때문에 부작용을 최소화할 수 있다는 큰 장점을 가지고 있다.2,3 그러나 이 시스템은 이식을 위한 잦은 반복적인 시술이 어렵기 때문에, 장기간의 방출 시간과 정교한 방출 특성 조절이 무엇보다도 중요하다.
최근 적층 제조 시스템, 즉 3D 프린팅을 이용해 약물 전달 시스템을 개발하려는 다양한 시도가 이루어지고 있다.4 3D 프린팅은 정교하고 복잡한 기하학적 구조의 제작을 통하여 방출 특성 조절 및 약물의 용량 조절이 용이하다.5,6 또한 2가지 이상의 약물을 동시에 사용하는 병용요법(Combination Therapy)을 위한 제형의 제작에도 적용이 가능하다.7,8 뿐만 아니라, 3D 프린팅 기술은 최근 각광받고 있는 개인 맞춤형 의학에 적합한 약물 전달 시스템의 제작에 매우 유용한 수단을 제공한다.9,10 이러한 3D 프린팅 기술의 유용성을 바탕으로 다양한 종류의 약물 전달 시스템들이 개발되고 있다. 예를 들어, FDM (Fused Deposition Modeling) 프린팅을 이용하여 여러 종류의 약물을 동시에 포함하며, 각 약물의 방출 시간을 조절할 수 있는 구강 투여용 약물 전달 시스템이 소개된 바 있다.11 또한, 레이저 기반 3D 프린팅 기술인 스테레오리소그래피(Stereolithography)와 3D 스캐너로 얻은 형상 데이터를 사용해 환자 맞춤형 여드름 치료 패치의 개발 결과도 보고된 바 있다.12 이와 같이 3D 프린팅 기술을 이용하여 다양한 종류의 약물 전달 시스템들이 개발되고 있지만, 장기간 조절 방출을 위한 이식형 약물 전달 시스템의 개발 사례는 매우 적다. 또한 재료의 가공을 위해 광개시제와 같은 독성이 있는 화학물질을 사용하지 않고, 전체 시스템을 모두 프린팅으로 제작한 사례는 아직 보고된 바 없다.
본 연구에서는 복합 3D 프린팅 기술을 이용하여 이식가능한 조절 방출형 약물 전달 시스템(Programmable Drug Delivery System)의 제작 가능성을 살펴보았다. 이를 위하여 마이크로 구조를 가지고 있는 이식형 캡슐을 디자인하였으며, 약물의 프린팅을 위한 하이드로젤 기반 바이오 잉크를 제작하였다. 그리고 생체 재료 및 디자인된 바이오 잉크를 이용한 복합 프린팅 공정을 통하여, 이식형 약물 전달 시스템을 제작하였다. 그 후 만들어진 캡슐의 마이크로 구조 및 하이드로젤의 농도가 약물 방출에 미치는 영향을 확인하기 위해 측정 및 분석을 수행하였다. 위의 과정을 통해 3D 프린팅 기술이 조절 방출형 약물 전달 시스템 개발에 활용될 수 있음을 확인하였다.
2. 3D 프린팅 시스템을 이용한 약물 전달용 캡슐 제작
2.1 3D 프린팅 시스템
본 연구에서는 약물 전달 시스템 제작을 위해 복합 3D 프린터(Hybrid 3D Printer)를 사용하였다(Fig. 1(a)). Fig. 1(b)와 같이, 복합 3D 프린팅 시스템은 3축 스테이지 시스템, 컨트롤러, 재료의 토출을 위한 디스펜싱 모듈 그리고 온도와 습도를 조절할 수 있는 인클로져로 구성되어 있다. 그 중 디스펜싱 모듈은 공압 또는 피스톤 기반의 토출 방식을 사용하는 총 6개의 프린팅 헤드들을 가지고 있다. 그리고 소프트웨어는 약물 전달 시스템의 디자인과 공정 설정이 가능한 코딩 프로그램과 시스템 제어 프로그램으로 구성되어 있다. 코딩 프로그램은 자체 개발되었으며, 시스템 제어 프로그램은 ㈜델타타우코리아의 CNC 소프트웨어를 이용하고 있다.
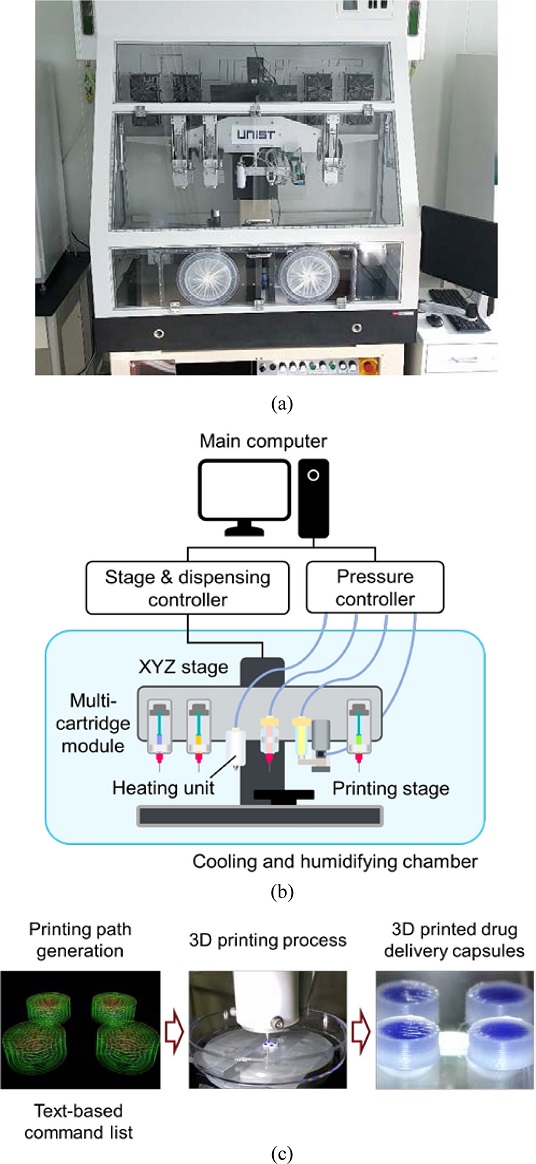
Hybrid 3D printing system. (a) Hybrid 3D printer. (b) Schematic of hybrid 3D printing system. (c) 3D printing process for drug delivery capsules
코딩 프로그램은 프린팅 패턴의 디자인뿐만 아니라 공기 압력, 토출 속도, 프린팅 속도의 조절 그리고 재료 변경 등이 가능하도록 개발되었다(Fig. 1(c)).13
2.2 약물 전달 시스템의 제작
본 연구에서 디자인된 약물 전달 시스템은 외부를 둘러싸는 캡슐과 약물이 내포된 하이드로젤로 구성되어 있다. 캡슐은 바이오 플라스틱인 Polycaprolactone (PCL) (Polysciences, USA)을 재료로 사용하며, 공압 방식의 프린팅 헤드를 통해 90oC, 780 KPa, 200 μm 노즐 그리고 80 mm/min의 이송 속도 조건에서 제작되었다. 또한 30% (w/v)의 Pluronic F127 하이드로젤과 모델 약물인 Brilliant Blue (BioRad Laboratories, USA)를 섞어 약물 전달용 하이드로젤 잉크를 제작하여 프린팅에 사용하였다.14 Pluronic F127 젤은 온도감응성 하이드로젤로 일정한 약물 방출 속도를 가지고 있어 주사형 약물 전달체로 많이 사용되고 있다.15,16 약물 전달 시스템의 제작에 사용된 30% (w/v)의 Pluronic F127 하이드로젤은 4oC의 콜드 룸에서 10 mL의 증류수에 3 g의 Pluronic F127 파우더(Sigma-Aldrich, USA)를 녹여 준비하였다. 그리고 준비된 10 mL의 Pluronic F127 용액에 0.05 g의 Brilliant Blue 파우더를 추가하여, 약물이 내포된 프린팅용 하이드로젤을 제작하였다. Pluronic F127 젤의 프린팅에는 피스톤 방식의 프린팅 헤드와 250 μm 노즐, 0.691 μL/sec의 토출 속도와 70 mm/min의 이송 속도 조건이 사용되었다. 그리고 프린팅 과정에서 젤의 점성변화를 막기 위해 인클로져의 내부 온도를 23oC로 유지하였다.
Table 1과 Fig. 2(a)는 본 연구에서 프린팅 된 약물 전달 시스템의 치수 정보와 디자인을 각각 보여주고 있다. 표와 그림에서 보는 바와 같이 캡슐은 직경 3.2 mm, 높이 1.4 - 2.6 mm의 원기둥 모양으로 제작되었으며, 상단 부 중앙에 약물이 방출되는 구멍을 가지고 있다. 구멍의 크기는 200 - 800 μm이며, 길이는 200 - 1,400 μm이다. 또한 캡슐 내부의 전체 하이드로젤 두께는 1,000 - 2,200 μm이며, 그 중 약물을 내포하고 있는 젤의 두께는 600 - 1,800 μm이다. 이와 같은 디자인의 캡슐을 만들기 위해 캡슐 1개당 약 7 - 13분의 제작시간이 소요되었다.
3. 약물 방출 특성 측정 및 분석
캡슐의 기하학적 구조와 하이드로젤의 농도 변경이 약물 방출에 주는 영향을 알아보기 위해 파라미터 스터디를 수행하였다. Table 1의 디자인을 기준으로, 캡슐 구멍의 지름과 길이, 약물이 내재된 하이드로젤의 두께 및 Pluronic F127 젤의 농도를 변화시키며 다양한 종류의 약물 전달 시스템을 제작하였다. 약물의 방출 실험은 제작된 시스템을 37oC의 2 mL PBS (pH 7.4)에 담근 후, 측정을 위해 용액을 샘플링 하였다. 그리고 자외선 및 가시광선 분광기(UV-Vis Spectrophotometer) (SpectraMax Plus 384, Molecular Devices, USA)를 사용해 560 nm의 파장에서 흡광도를 측정하였다. 그 다음 Standard Curve를 통해 각 샘플의 농도를 구하였으며 이를 바탕으로 방출된 약물의 양을 계산하였다. 또한 이를 처음부터 순차적으로 더해 방출된 약물의 총량을 구하고 분석에 활용하였다.
3.1 구멍의 직경에 따른 약물 방출 특성 변화
약물이 방출되는 구멍의 지름 변화가 미치는 영향을 확인하기 위해 200 μm, 500 μm 그리고 800 μm 크기의 구멍을 가진 캡슐을 제작하였다(Fig. 3(a)). Fig. 3(b)는 시간에 따른 약물의 방출량을 보여주고 있다. 그래프에서 보는 바와 같이 200 μm의 구멍 크기를 가진 캡슐은 7일 동안 비교적 일정한 방출 속도를 보였으며, 500 μm와 800 μm 그룹은 초반 버스트 방출(Burst Release)이 관찰되었다. 위의 결과를 통해 캡슐 구멍의 지름이 커질수록 초반 방출 속도가 증가하였음을 확인하였다.
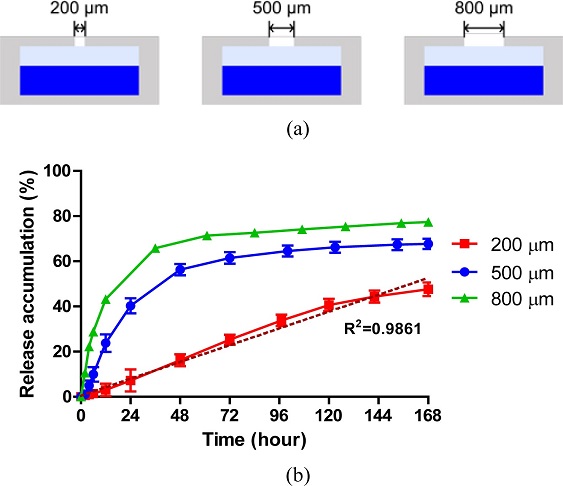
3D printed capsules with varying orifice diameters. (a) Schematic of capsules with 200 μm, 500 μm, and 800 μm hole sizes. (b) In vitro model drug release profile of the capsular devices (mean ± standard deviation, n = 4)
이는 구멍 크기의 증가가 하이드로젤과 PBS 용액이 접촉하는 면적을 증가시켜, 방출 속도를 증가시킨 것이다. 800 μm의 구멍 크기를 가진 캡슐의 경우, 약 24시간 동안 전체의 50%에 해당하는 약물이 방출되었으며, 500 μm 그룹의 경우 약 50%의 약물이 방출되기까지 약 36시간이 걸렸다. 반면에 500 μm와 800 μm그룹 모두 방출된 약물이 50 - 60%가 넘어가면 방출 속도가 점차 감소하는 것이 확인되었다.
약물 전달을 위해 캡슐 없이 Pluronic F127 하이드로젤을 바로 사용한 기존의 시스템들은 단 몇 시간 만에 모든 방출이 이루어졌다.15,16 하지만 본 연구에서 개발된 약물 전달 시스템은 소량의 하이드로젤을 사용하였음에도 7일동안 방출이 지속되었으며, 200 μm 그룹의 경우에는 7일동안 50% 이하의 방출량을 보여주었다. 이는 PCL 캡슐이 PBS 용액으로부터 하이드로젤이 빠르게 녹는 것을 보호하고 마이크로 크기의 구멍을 통해서만 약물 방출이 허용되었기 때문이다.
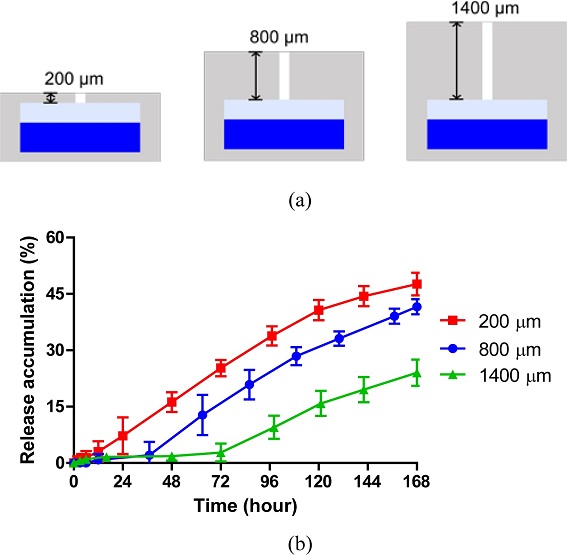
3.2 구멍의 길이에 따른 약물 방출 특성 변화
약물 전달 캡슐의 구멍의 길이가 방출 특성에 미치는 영향을 확인하기 위해, 구멍의 지름을 200 μm로 고정하고 길이가 200 μm, 800 μm 그리고 1,400 μm인 샘플을 제작하였다(Fig. 4(a)). 7일동안 캡슐에서 방출된 약물의 누적량을 측정한 결과 800 μm와 1,400 μm의 구멍 길이를 가진 캡슐에서 각각 36시간과 72시간의 지연 후에 방출이 시작되는 것이 관찰되었다(Fig. 4(b)). 또한 약물 방출이 시작된 뒤 두 그룹 그래프의 기울기는 각각 0.2949와 0.2226으로, 0.3101의 기울기를 가진 200 μm 그룹과 비슷한 기울기의 그래프 계형을 보여주었다. 게다가 800 μm 그룹과 1,400 μm 각각 0.9828과 0.9876의 R2 값을 보여 거의 균일한 속도로 약물이 방출됨을 확인하였다. 뿐만 아니라, 구멍의 길이가 600 μm 증가할 때 마다 약 36시간씩 방출 시간이 지연된 것을 확인할 수 있었다. 이는 소수성 고분자이자 캡슐의 재료인 PCL의 영향으로, 결론적으로 캡슐 구멍의 길이가 증가할수록 약물 전달이 시작되는 시점이 지연되는 것으로 확인되었다.
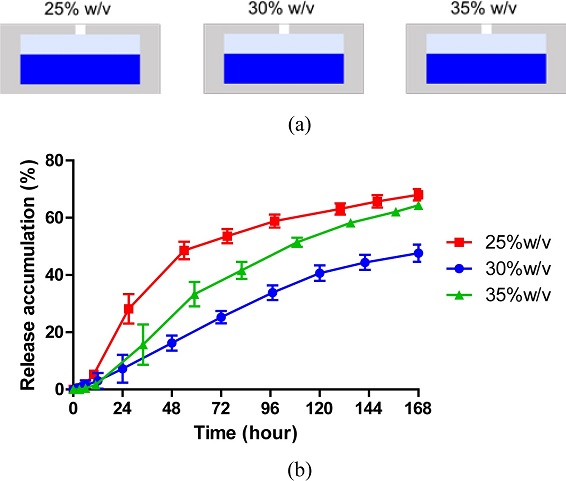
3.3 Pluronic F127 젤의 농도에 따른 약물 방출 특성 변화
약물을 전달하는 하이드로젤의 농도가 약물 방출 특성에 미치는 영향을 확인하기위해 25% (w/v), 30% (w/v) 그리고 35% (w/v) 농도의 하이드로젤을 이용해 샘플을 제작하였다(Fig. 5(a)). 실험결과 비교적 일정한 속도로 약물을 방출했던 30% (w/v) 그룹과 달리, 25% (w/v)와 35% (w/v) 그룹은 초반에 약물이 빠른 속도로 방출되었다가 중반부터 속도가 줄어들었다(Fig. 5(b)). 특히 25% (w/v) 그룹의 경우, PBS에 의해 젤이 녹는 속도가 타 그룹에 비해 빨라, 다른 그룹에 비해 빠른 약물 방출을 보였다.14 그 결과, 25% (w/v) 농도의 젤을 사용한 그룹은 약 48시간동안 전체의 50%에 가까운 약물을 방출한 것으로 측정되었다. 반면 35% (w/v) 그룹의 경우 고분자의 높은 농도로 인한 하이드로젤의 심한 팽창으로 캡슐 밖으로 재료가 토출 되는 현상이 관찰되었다.17 이러한 토출 현상으로 기존의 시스템과 다른 경향성을 가지는 약물 전달 특성이 형성되었다. 또한 이 그룹은 약 60시간이 지난 후에는 약물의 방출 속도가 줄어 30% (w/v) 그룹과 비슷한 속도로 약물이 방출됨을 확인할 수 있었다.
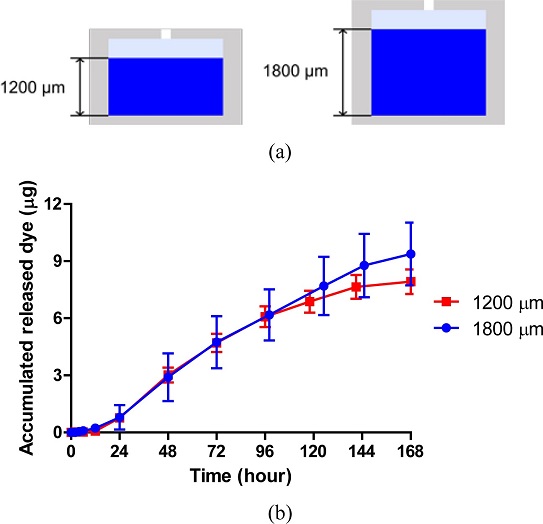
3.4 약물이 내재된 하이드로젤의 두께 변화에 따른 약물 방출 특성 변화
약물이 포함된 젤의 두께가 방출 특성에 미치는 영향을 확인하기 위해, 모델 약물인 Brilliant Blue가 포함된 30% (w/v) 하이드로젤의 두께가 각각 1,200 μm와 1,800 μm인 샘플을 제작하였다(Fig. 6(a)). 7일 동안 약물 방출 실험을 수행한 결과 두 그룹이 유사한 방출 속도를 가지는 것을 확인할 수 있었다(Fig. 6(b)). 4일 동안에는 두 그룹의 방출 속도가 거의 동일 하였으며, 그 이후에는 1,200 μm 그룹에서 약간 감소하는 것이 관찰되었다. 그러나 7일째 데이터에서는 두 그룹 간의 통계적 유의성은 관찰되지 않았다. 결론적으로 약물이 포함된 젤의 두께는 약물의 방출 특성에 큰 영향을 미치지 않는 다는 것을 확인할 수 있었다. 따라서 본 시스템의 길이를 증가시켜 이식을 위한 긴 원통형의 캡슐을 제작해도 기존 시스템과 비슷한 성능을 구현할 수 있다.
4. 결론
본 연구에서는 복합 3D 프린팅 기술을 이용하여 7일 이상 서방형 방출이 가능한 약물 전달 시스템을 개발하였다. 그 결과, 제작된 캡슐의 구조와 약물을 전달하는 하이드로젤의 농도 등을 변경하여 약물 방출의 속도, 프로파일 개형뿐만 아니라 방출 시작을 지연시켜 방출이 시작되는 시점까지 조절할 수 있음을 확인했다. 또한 약물이 포함된 하이드로젤의 양이 증가해도 비슷한 방출 속도를 가진다는 것을 확인하였으며, 이를 통해 다양한 용량의 약물을 포함하는 약물 전달 시스템의 제작 가능성을 볼 수 있었다. 본 연구에서 개발된 약물 전달 시스템은 호르몬과 성장인자 및 단백질 치료제를 포함하는 다양한 약물을 국소 부위에 전달하기 위한 이식형 시스템으로 활용할 수 있다. 그리고 무엇보다도 치료 목적에 따라 시스템의 약물 방출 특성을 자유자제로 조절할 수 있기 때문에, 이러한 장점을 통해 다양한 질병에 대한 효과적인 치료 기술의 개발에 큰 효용성을 줄 것이다.
Acknowledgments
이 논문은 2018년도 정부(미래창조과학부)의 재원으로 한국연구재단 바이오·의료기술개발사업의 지원을 받아 수행된 연구임(No. 2017M3A9C6033135 and No. 2015M3A9B3028685).
REFERENCES
-
Allen, T. M. and Cullis, P. R., “Drug Delivery Systems: Entering the Mainstream,” Science, Vol. 303, No. 5665, pp. 1818-1822, 2004.
[https://doi.org/10.1126/science.1095833]

-
Brem, H., “Polymers to Treat Brain Tumours,” Biomaterials, Vol. 11, No. 9, pp. 699-701, 1990.
[https://doi.org/10.1016/0142-9612(90)90030-T]

-
Fung, L. K. and Saltzman, W. M., “Polymeric Implants for Cancer Chemotherapy,” Advanced Drug Delivery Reviews, Vol. 26, Nos. 2-3, pp. 209-230, 1997.
[https://doi.org/10.1016/S0169-409X(97)00036-7]

-
Zema, L., Melocchi, A., Maroni, A., and Gazzaniga, A., “Three-Dimensional Printing of Medicinal Products and the Challenge of Personalized Therapy,” Journal of Pharmaceutical Sciences, Vol. 106, No. 7, pp. 1697-1705, 2017.
[https://doi.org/10.1016/j.xphs.2017.03.021]

-
Kyobula, M., Adedeji, A., Alexander, M. R., Saleh, E., Wildman, R., et al., “3D Inkjet Printing of Tablets Exploiting Bespoke Complex Geometries for Controlled and Tuneable Drug Release,” Journal of Controlled Release, Vol. 261, pp. 207-215, 2017.
[https://doi.org/10.1016/j.jconrel.2017.06.025]

-
Pietrzak, K., Isreb, A., and Alhnan, M. A., “A Flexible-Dose Dispenser for Immediate and Extended Release 3D Printed Tablets,” European Journal of Pharmaceutics and Biopharmaceutics, Vol. 96, pp. 380-387, 2015.
[https://doi.org/10.1016/j.ejpb.2015.07.027]

-
Khaled, S. A., Burley, J. C., Alexander, M. R., Yang, J., and Roberts, C. J., “3D Printing of Five-in-One Dose Combination Polypill with Defined Immediate and Sustained Release Profiles,” Journal of Controlled Release, Vol. 217, pp. 308-314, 2015.
[https://doi.org/10.1016/j.jconrel.2015.09.028]

-
Khaled, S. A., Burley, J. C., Alexander, M. R., Yang, J., and Roberts, C. J., “3D Printing of Tablets Containing Multiple Drugs with Defined Release Profiles,” International Journal of Pharmaceutics, Vol. 494, No. 2, pp. 643-650, 2015.
[https://doi.org/10.1016/j.ijpharm.2015.07.067]

-
Sandler, N. and Preis, M., “Printed Drug-Delivery Systems for Improved Patient Treatment,” Trends in Pharmacological Sciences, Vol. 37, No. 12, pp. 1070-1080, 2016.
[https://doi.org/10.1016/j.tips.2016.10.002]

-
Trenfield, S. J., Awad, A., Goyanes, A., Gaisford, S., and Basit, A. W., “3D Printing Pharmaceuticals: Drug Development to Frontline Care,” Trends in Pharmacological Sciences, Vol. 39, No. 5, pp. 440-451, 2018.
[https://doi.org/10.1016/j.tips.2018.02.006]

-
Maroni, A., Melocchi, A., Parietti, F., Foppoli, A., Zema, L., et al., “3D Printed Multi-Compartment Capsular Devices for Two-Pulse Oral Drug Delivery,” Journal of Controlled Release, Vol. 268, pp. 10-18, 2017.
[https://doi.org/10.1016/j.jconrel.2017.10.008]

-
Goyanes, A., Det-Amornrat, U., Wang, J., Basit, A. W., and Gaisford, S., “3D Scanning and 3D Printing as Innovative Technologies for Fabricating Personalized Topical Drug Delivery Systems,” Journal of Controlled Release, Vol. 234, pp. 41-48, 2016.
[https://doi.org/10.1016/j.jconrel.2016.05.034]

-
Kang, H.-W., Lee, S. J., Ko, I. K., Kengla, C., Yoo, J. J., et al., “A 3D Bioprinting System to Produce Human-Scale Tissue Constructs with Structural Integrity,” Nature Biotechnology, Vol. 34, No. 3, pp. 312.-319, 2016.
[https://doi.org/10.1038/nbt.3413]

-
Shu, X. and Zhu, K., “The Release Behavior of Brilliant Blue from Calcium–Alginate Gel Beads Coated by Chitosan: The Preparation Method Effect,” European Journal of Pharmaceutics and Biopharmaceutics, Vol. 53, No. 2, pp. 193-201, 2002.
[https://doi.org/10.1016/S0939-6411(01)00247-8]

-
Zhang, L., Parsons, D. L., Navarre, C., and Kompella, U. B., “Development and In-Vitro Evaluation of Sustained Release Poloxamer 407 (P407) Gel Formulations of Ceftiofur,” Journal of Controlled Release, Vol. 85, Nos. 1-3, pp. 73-81, 2002.
[https://doi.org/10.1016/S0168-3659(02)00273-0]

-
Liu, Y., Lu, W.-L., Wang, J.-C., Zhang, X., Zhang, H., et al., “Controlled Delivery of Recombinant Hirudin Based on Thermo-Sensitive Pluronic® F127 Hydrogel for Subcutaneous Administration: In Vitro and In Vivo Characterization," Journal of Controlled Release, Vol. 117, No. 3, pp. 387-395, 2007.
[https://doi.org/10.1016/j.jconrel.2006.11.024]

- Camana G. and Tavano M., “Synthesis and Characterisation of Pluronic Hydrogels for Biomedical Applications,” M.Sc Thesis, School of Industrial and Information Engineering, Politecnico Di Milano, 2014.