에어나이프 시스템을 이용한 3차원 복합 형상 PDMS 마이크로스텐실 제작 및 세포배양 응용
Copyright © The Korean Society for Precision Engineering
This is an Open-Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
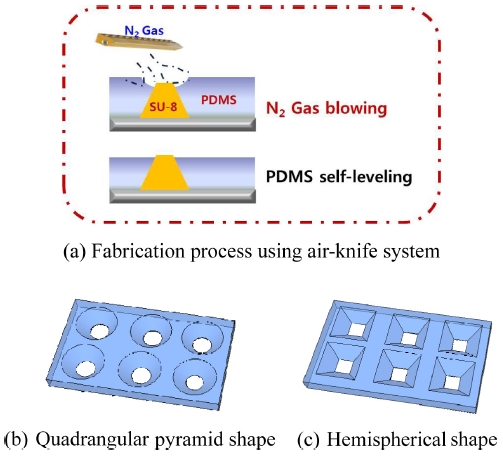
In this study, we propose a fabrication method of three-dimensional complex shape polydimethylsiloxane microstencils. Three-dimensional complex shape polydimethylsiloxane (PDMS) microstencils were fabricated by an air-knife system and PDMS casting form preparing master mold by photolithography, diffuser lithography and polyurethane acrylate (PUA) replication. PDMS microstencils shape was a production of the hemispherical and quadrangular pyramid. When the prepolymer of PDMS was spin-coated onto the three-dimensional complex shape master mold, a thin layer of prepolymer remained on top of the master's structure and consequently prevented formation of perforated patterns. This residual layer was easily removed by the air-knife. The air-knife system was controlled by the flow rate of N2 gas and conveying speed of the master mold. Results revealed the fabricated three-dimensional complex shape PDMS microstencils, could be useful for application of three-dimensional cell culture device.
Keywords:
Air-knife system, PDMS microstencil, Three-dimensional complex shape키워드:
에어나이프 시스템, PDMS 마이크로스텐실, 3차원 복합 형상1. 서론
2000년 이후 마이크로스텐실을 이용한 2차원 형태의 마이크로 패턴 제작과 이를 응용한 마이크로 패턴 형상으로 세포를 배양하는 연구가 진행되었다. 마이크로 패턴 세포배양은 세포를 국부적인 영역에서 제어된 미세환경을 제공하여 세포를 배양하는 방법으로 국부적으로 배양된 세포의 위치, 크기 등을 정확하게 제어함으로써 체계적이고 공학적인 세포연구를 가능하게 한다. 이러한 마이크로 패턴 세포배양은 2차원 표면 패터닝을 통한 세포의 점착을 국부화 함으로써 세포를 배양하는 방법으로 In Vitro 세포연구에 다양한 정보를 제공한다.1-7 그러나 대부분의 실제 세포들은 체내에서 3차원 형태로 배양되며, 이를 모사하는 새로운 구조체와 3차원 형상을 갖는 생체기관을 모사한 세포배양으로 생물체의 반응을 정확하게 재현하기 위한 새로운 형태의 세포배양 기술에 관한 연구가 많은 연구진에 의해 수행되고 있다.8-10
생체적합성 고분자(Polydimethylsiloxane, PDMS)로 제작되는 일반적인 마이크로스텐실은 미세유체 챔버(Microfluidic Chamber)와 미세구멍에 연결된 주사기(Syringe)로 PDMS 중합체를 흡입하여 제작하거나 반대로 PDMS 중합체가 도포된 마스터 몰드 위로 가압(Pressure)이 가능한 판을 이용하여 제작되었다.1,2,4,11 그러나 이러한 제작 방법은 대면적 스텐실 제작의 어려움과 스텐실 제작 수율(스텐실의 관통 확률)이 낮은 단점을 가진다. 또한, 흡입공정으로 제작할 경우 흡입속도에 따른 미세 공기가 마이크로 패턴 뒤로 갇히는 문제가 발생하며 이를 해결하기 위한 흡입속도 및 압력 조절이 가능한 외부장치가 필요하다. 가압공정으로 제작할 경우 동일한 압력으로 가압판을 누르는 외부장치가 필요하며, 압력이 불균일할 경우 마이크로 패턴에 얇은 막이 생성되어 건식식각(Dry Etching)과 습식식각(Wet Etching) 등과 같은 후처리 공정이 요구된다.
최근 새로운 PDMS 마이크로스텐실 제작 방법으로 가스블로잉(Gas Blowing)12,13을 이용한 방법과 에어나이프(Air-Knife) 시스템을 사용한 마이크로스텐실 제작 자동화 시스템14에 관한 연구가 보고되었다. 가스블로잉 방법은 질소가스(Nitrogen Gas)를 마스터 몰드 위로 분사하여 마이크로 패턴 위 잔류 PDMS 층을 제거하는 방법이며, 에어나이프 시스템을 사용한 자동화 시스템은 자동 이송장치와 질소가스의 대면적 분사가 가능한 에어나이프를 사용하여 마스터 몰드의 잔류 PDMS 층을 대면적 분사를 통해 자동화 시스템으로 직접 제거하는 방법이다. 이러한 가스분사식 마이크로스텐실 제작 방법은 PDMS 잔류층을 쉽고 빠르게 제거 가능하고 제작시간 단축 및 추가 장비 없이 대면적의 PDMS 마이크로스텐실을 쉽게 제작할 수 있는 장점을 가진다. 또한, 에어나이프를 사용한 가스분사식 자동화 시스템은 일반적인 가스블로잉 제작 방법의 기술적 한계인 숙련도에 의한 재현성, 고분자 스텐실 형상 제어 등의 단점을 개선한 마이크로스텐실 제작 방법으로 롤투롤(Roll to Roll) 공법과 함께 대량생산이 가능한 새로운 형태의 자동화 공법이다.
본 연구에서는 에어나이프를 사용한 PDMS 마이크로스텐실 제작 자동화 시스템의 높은 생산성 및 정량화된 제조 기술과 3차원 복합 형상을 갖는 마스터 몰드 제작 기술을 결합하여 3차원 복합 형상을 갖는 다양한 형상의 PDMS 마이크로스텐실을 제작하는 기술을 개발하고, 이를 3차원 형상을 갖는 세포배양 시스템으로 적용하여 In Vitro 세포연구의 새로운 형태인 3차원 세포배양기술에 관한 연구를 수행하였다.
2. 마스터 몰드 제작
3차원 복합 형상을 갖는 마스터 몰드는 음성감광제인 SU-8 포토레지스트와 디퓨져리소그라피15,16 공정을 사용하여 제작된 반구형상 마스터 몰드, 실리콘 웨이퍼를 직접 식각하고 광경화성 고분자인 PUA (Polyurethane Acrylate)로 복제하여 제작된 사각뿔형 마스터 몰드 두 종류를 제작한다. Fig. 1은 제작된 두 종류의 마스터 몰드 이미지이다.

(a) Optical image of hemispherical shape master mold, (b) SEM image of quadrangular pyramid shape master mold
디퓨져리소그라피 공정으로 제작된 반구형상 마스터 몰드는 PDMS와의 분리가 용이하도록 실렌(Tridecafluoro-1,1,2,2-Tetrahydrooctyl-1-Trichlorosilane) 으로 표면처리 후 PDMS 중합체와 에어나이프 시스템을 사용하여 반구형 마이크로스텐실을 제작한다.14-16 반구형 마스터 몰드 제작과정은 마이크로 패턴이 새겨진 크롬마스크에 SU-8 감광제를 도포하고 베이킹 과정을 거친 후 오팔 디퓨저시트를 이용하여 자외선을 산란시켜 제작한다. 사각뿔형 마스터 몰드는 마이크로 패턴이 형성된 실리콘 웨이퍼를 KOH를 이용한 Wet Etching 방법으로 직접 식각하여 제작하고 실렌으로 표면처리 후 PDMS 중합체를 이용하여 반대형상의 PDMS 몰드를 복제한다. 복제된 PDMS 몰드는 다시 광경화성 고분자인 PUA를 이용하여 실리콘 웨이퍼와 동일한 형상으로 복제하여 PUA 사각뿔형 마스터 몰드를 제작한다. 제작된 PUA 마스터 몰드와 에어나이프 시스템을 이용하여 사각뿔형 마이크로스텐실을 제작한다. 광경화성 고분자인 PUA로 제작된 마스터 몰드는 PDMS와 분리가 용이하며, 쉽고 빠르게 미세패턴 복제가 가능한 장점을 가진다. 본 연구에서는 실리콘 웨이퍼를 직접 식각하여 제작된 사각뿔형 마스터 몰드가 아닌 PUA 복제 마스터 몰드를 사용하여 3차원 복합 형상 마이크로스텐실을 제작한다.
3. 에어나이프 시스템을 이용한 3차원 복합형상 PDMS 마이크로스텐실
3차원 구조를 갖는 PDMS 마이크로스텐실은 에어나이프 시스템 자동화 장치를 사용하여 제작한다. Fig. 2는 3차원 복합 형상 PDMS 마이크로스텐실의 제작공정과 개략도를 보여주며, Fig. 3은 실험에 직접 사용된 에어나이프가 결합된 마이크로스텐실 제작 자동화 시스템이다. 제작된 3차원 복합 형상 PDMS 마이크로스텐실은 Fig. 3의 에어나이프 시스템과 Fig. 1의 3차원 복합형상을 갖는 두 종류의 마스터 몰드를 이용하여 제작한다.
Fig. 3의 에어나이프 시스템은 질소가스의 분사에 사용되는 에어나이프(Air Knife; NEX FLOWTM), 에어 나이프의 높이를 제어하는 Z축 전동 스테이지(Motorized Stage), 마스터 몰드의 이송속도를 제어하는 X축 전동 스테이지, 2축 제어용 컨트롤러로 구성된다. X축 전동 스테이지에는 2개의 리미트 센서(Limit Sensor)와 1개의 홈 센서(Home Sensor)를 장착하여 이송속도 및 이송거리를 제어할 수 있으며, 마스터 몰드를 올릴 수 있는 평판(150 × 150 mm)이 장착되어 있다. Z축 전동 스테이지는 에어 나이프 결합이 가능한 지그(Jig)가 장착되어 있다. 그리고, 질소가스의 압력(MPa)과 유량(L/min)을 조정하기 위해 질소탱크의 출구에 레귤레이터(Regulator)를 장착하였다. Fig. 3 오른쪽 상단의 이미지는 마스터 몰드가 장착된 이송용 평판과 에어나이프를 통해 질소가스가 마스터 몰드 위로 분사되는 이미지이다. 에어나이프를 통해 분사된 질소가스는 마이크로 패턴 위의 PDMS 중합체를 밀어내어 관통형상의 마이크로 스텐실을 제작한다. (Fig. 2(a)) 에어나이프 시스템이 결합된 자동화 장치를 이용한 마이크로스텐실 제작 공정조건은 다음과 같다.14 마스터 몰드의 이송속도 100 mm/min, 질소의 압력 0.4 MPa, 질소의 유량 15 L/min 그리고 밑면의 마스터 몰드와 Z축 전동 스테이지에 장착된 에어나이프 사이의 간격 5 mm이다. Fig. 4는 사각뿔형상의 3차원 복합 형상을 갖는 PDMS 마이크로스텐실의 제작 후 이미지를 확인한 결과이며, Fig. 5는 제작된 반구형상의 3차원 복합 형상을 갖는 PDMS 마이크로스텐실의 실제 이미지이다. 두 종류의 3차원 복합 형상을 갖는 PDMS 마이크로스텐실을 제작하고 이를 현미경을 이용하여 확인한 결과 마이크로 패턴 위쪽 부분이 관통됨을 확인할 수 있다.
4. 실험결과 분석 및 세포배양 응용
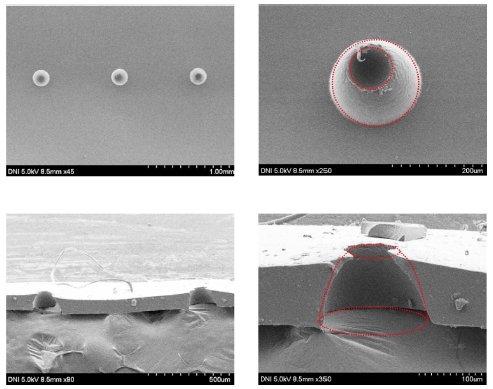
제작된 3차원 복합 형상PDMS 마이크로스텐실 단면의 형상 및 크기 확인을 위해 전자주사현미경(Scanning Electron Microscope, SEM)을 이용하여 측정하였다. 측정결과 Fig. 6의 사각뿔형 PDMS 마이크로스텐실은 마이크로 패턴의 모서리에서 PDMS가 얇아지고 갈라지는 현상이 관찰되었다. 이러한 현상은 마이크로 패턴에서 벽면과 모서리에서의 PDMS 부착력의 차이에 의해 발생하는 현상으로 PDMS가 면적이 넓은 부분에서는 부착이 쉽기 때문에 벽면을 올라가면서 굳어지며 반면에 면적이 작은 모서리 부분에서는 부착이 어렵기 때문에 넓은 면적에 비해 높이가 낮아지는 현상을 관찰할 수 있다. Fig. 7은 반구형상 PDMS 마이크로스텐실의 SEM 측정결과로 PDMS 단면을 확인한 결과 사각뿔형상 PDMS 마이크로스텐실에서 나타난 현상이 관찰되지 않았으며, 마이크로 패턴 사이(피치)의 PDMS 두께가 일정한 것을 확인할 수 있다. 두 종류의 마이크로 패턴을 이용한 실험결과를 분석하면 사각뿔형상 PDMS 마이크로스텐실에서 나타나는 현상을 해결하기 위해서는 3차원 마이크로 패턴의 형상을 원뿔형상으로 제작하거나 마이크로 패턴의 모서리 경계 각도를 줄이는 것이 두께가 일정한 PDMS 마이크로스텐실 제작에 도움이 될 것으로 판단된다.
제작된 사각뿔형상의 3차원 PDMS 마이크로스텐실(밑면 200 μm, 윗면 800 μm, 높이 420 μm)은 간세포(HepG2 Cell)의 3차원 배양으로 응용하였다. 실험과정은 다음과 같다. 멸균 처리된 세포배양용 글라스와 사각뿔형 PDMS 마이크로스텐실을 결합하고, 이를 다시 산소 플라즈마 장치를 이용하여 표면개질 시킨다. 산소 플라즈마를 이용한 표면개질은 PDMS 마이크로스텐실의 소수성 표면을 친수성으로 변화시켜 세포와 배양액이 안정적으로 침투되도록 하기 위해서 표면처리 공정을 시행한다. 표면개질 된 세포배양용 글라스 및 PDMS 마이크로스텐실은 PEG (Poly Ethylene Glycol)를 코팅하고 세척과 건조과정을 거친 후 다시 산소플라즈마 처리하여 세포배양에 사용한다. 간세포는 바닥에 붙어서 자라는 부착특성을 가진 세포로 부착특성을 억제하여 3차원 형상으로 배양하기 위해 세포배양용 글라스와 PDMS 마이크로스텐실에 PEG 코팅을 시행한다.17 준비된 세포배양 샘플에 간세포 배양액과 간세포를 넣고 인큐베이터 안에서 배양한다. 세포배양액을 넣는 과정에서 발생하는 마이크로 버블은 피펫팅을 이용하여 쉽게 제거가 가능하며, 마이크로 버블 제거 후 간세포를 넣고 배양액을 추가하는 과정을 거쳐 7일간 배양한다. 7일간 배양된 간세포의 측정은 공초점 현미경(Confocal Microscopy) 을 이용하였다. Fig. 8 은 공초점 현미경으로 측정된 간세포의 3차원 이미지를 보여주고 있다. 측정결과 3차원 형상으로 7일간 배양된 간세포는 사각뿔형 PDMS 마이크로스텐실이 제공하는 물리적 배양공간의 크기와 모양에 따라 간세포가 뭉쳐서 배양되었으며, 간세포의 크기는 높이 420 μm보다 낮고 바닥 크기인 200 μm보다 큰 형태로 배양됨을 확인할 수 있다. 배양된 간세포는 크기 300 μm, 높이 300 μm를 가지며 사각뿔형 PDMS 마이크로스텐실 안에서 3차원 형태로 배양되었다.
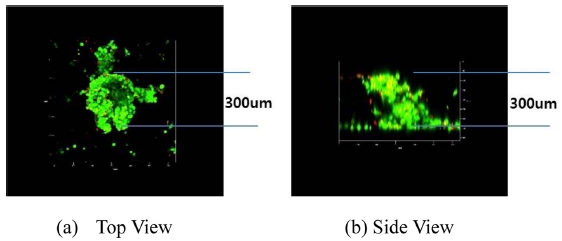
Fluorescent confocal image of HepG2 cell 3D culture using quadrangular pyramid shape PDMS microstencil (LIVE/DEAD® assay: Live cells stained green; dead cells stained red)
또한, 기존의 간세포 배양방식과는 다르게 새로운 형태의 3차원 세포배양기술로 간세포의 부착성질을 억제를 위해 PEG 코팅을 사용하였고, 배양과정에서 간세포가 뭉쳐서 배양될 수 있도록 3차원 구조를 갖는 PDMS 마이크로스텐실의 물리적 공간을 제공함으로써 간세포가 3차원 형상으로 뭉쳐서 배양이 가능하였다.
7일간 배양된 간세포의 생존여부 측정을 위해서 LIVE/DEAD® Assay Kit를 활용하였다. Fig. 8의 공초점 현미경으로 측정된 형광이미지를 보면 녹색형상의 둥근 모양을 확인할 수 있으며, 이는 간세포가 살아서 배양되고 있음을 보여주는 결과이다. LIVE/DEAD® Assay Kit는 형광이지를 이용하여 세포의 생존여부를 판단하는 지시약으로 녹색은 살아있는 세포, 적색은 죽은 세포를 나타낸다. 공초점 현미경의 형광이미지 분석결과 7일간 배양된 간세포는 3차원 형상으로 둥글게 뭉쳐서 생존되고 있음을 확인할 수 있다.
5. 결론
본 연구에서는 가스블로잉을 이용한 PDMS 마이크로스텐실 제작의 단점인 숙련도에 의한 재현성, 고분자 스텐실 형상 제어 등의 문제점를 개선한 PDMS 마이크로스텐실 제작 자동화 장치를 사용하여 높은 생산성과 정량화된 제조 기술을 확보하였다. 또한 3차원 복합 형상을 갖는 마스터 몰드 제작 기술을 활용하여 다양한 입체형상을 갖는 마스터 몰드를 제작하고, 이를 이용하여 고분자 마이크로스텐실을 3차원 복합 형상을 갖는 PDMS 마이크로스텐실로 제작하는 기술을 개발하였다.
제작된 3차원 복합 형상을 갖는 PDMS 마이크로스텐실은 마이크로 패턴 세포배양 기술과 차별화된 새로운 형태의 3차원 세포배양기술로 응용이 가능하였으며, 본 연구에서는 간세포를 3차원 형상으로 직접 배양 후 공초점 현미경을 이용하여 간세포 형상측정 및 생존을 확인하여 새로운 형태의 3차원 세포배양기술의 실효성을 검증하였다.
본 연구에서 제안한 3차원 세포배양기술은 향후 마이크로 유체 장치와 결합하여3차원 세포배양이 가능한 Cell on a Chip 시스템으로 활용 가능할 것으로 예상된다.
Acknowledgments
본 연구는 미래창조과학부의 재원으로 한국연구재단의 지원(NRF-2015R1C1A1A01055210)을 받아 수행되었음.
REFERENCES
-
Folch, A., Jo, B.-H., Hurtado, O., Beebe, D. J., and Toner, M., “Microfabricated Elastomeric Stencils for Micropatterning Cell Cultures,” Journal of Biomedical Materials Research, Vol. 52, No. 2, pp. 346-353, 2000.
[https://doi.org/10.1002/1097-4636(200011)52:2<346::AID-JBM14>3.0.CO;2-H]

-
Tourovskaia, A., Barber, T., Wickes, B. T., Hirdes, D., Grin, B., et al., “Micropatterns of Chemisorbed Cell Adhesion-Repellent Films Using Oxygen Plasma Etching and Elastomeric Masks,” Langmuir, Vol. 19, No. 11, pp. 4754-4764, 2003.
[https://doi.org/10.1021/la0267948]

-
Khetani, S. R. and Bhatia, S. N., “Microscale Culture of Human Liver Cells for Drug Development,” Nature Biotechnology, Vol. 26, No. 1, pp. 120-126, 2008.
[https://doi.org/10.1038/nbt1361]

-
Cho, C. H., Park, J., Tilles, A. W., Berthiaume, F., Toner, M., et al., “Layered Patterning of Hepatocytes in Co-Culture Systems Using Microfabricated Stencils,” Biotechniques, Vol. 48, No. 1, p. 47, 2010.
[https://doi.org/10.2144/000113317]

-
Choi, J. H., Lee, H., Jin, H. K., Bae, J.-S., and Kim, G. M., “Micropatterning of Neural Stem Cells and Purkinje Neurons Using a Polydimethylsiloxane (PDMS) Stencil,” Lab on a Chip, Vol. 12, No. 23, pp. 5045-5050, 2012.
[https://doi.org/10.1039/c2lc40764g]

-
Choi, J. H., Lee, H., Jin, H. K., Bae, J.-S., and Kim, G. M., “Fabrication of Microengineered Templates and their Applications into Micropatterned Cell Culture,” Journal of Biomedical Nanotechnology, Vol. 9, No. 3, pp. 377-381, 2013.
[https://doi.org/10.1166/jbn.2013.1508]

-
Choi, J. H., Jin, H. K., Bae, J.-S., Park, C. W., Cheong, I. W., et al., “Fabrication of Detachable Hydrogel Microplates for Separably Patterned Cell Culture,” Int. J. Precis. Eng. Manuf., Vol. 15, No. 5, pp. 945-948, 2014.
[https://doi.org/10.1007/s12541-014-0421-y]

-
Morimoto, Y., Tsuda, Y., and Takeuchi, S., “Reconstruction of 3D Hierarchic Micro-Tissues Using Monodisperse Collagen Microbeads,” Proc. of the International Conference on Micro Electro Mechanical Systems, pp. 56-59, 2009.
[https://doi.org/10.1109/MEMSYS.2009.4805318]

-
Shin, Y., Han, S., Jeon, J. S., Yamamoto, K., Zervantonakis, I. K., et al., “Microfluidic Assay for Simultaneous Culture of Multiple Cell Types on Surfaces or Within Hydrogels,” Nature Protocols, Vol. 7, No. 7, pp. 1247-1259, 2012.
[https://doi.org/10.1038/nprot.2012.051]

-
Yeon, S.-E., Lee, S.-H., Nam, S. W., Oh, I.-H., Lee, J., et al., “Application of Concave Microwells to Pancreatic Tumor Spheroids Enabling Anticancer Drug Evaluation in a Clinically Relevant Drug Resistance Model,” PLOS One, Vol. 8, No. 9, Paper No. E73345, 2013.
[https://doi.org/10.1371/journal.pone.0073345]

-
Choi, J. H. and Kim, G. M., “Micro-Patterning on Non-Planar Surface Using Flexible Microstencil,” Int. J. Precis. Eng. Manuf., Vol. 12, No. 1, pp. 165-168, 2011.
[https://doi.org/10.1007/s12541-011-0023-x]

-
Kang, J. H., Um, E., and Park, J.-K., “Fabrication of a Poly (Dimethylsiloxane) Membrane with Well-Defined Through-Holes for Three-Dimensional Microfluidic Networks,” Journal of Micromechanics and Microengineering, Vol. 19, No. 4, Paper No. 045027, 2009.
[https://doi.org/10.1088/0960-1317/19/4/045027]

-
Choi, J. H. and Kim, G. M., “Fabrication of PDMS Stencil Using Gas Blowing for Micropatterned 3T3 Cell Culture,” J. Korean Soc. Precis. Eng., Vol. 30, No. 2, pp. 236-240, 2013.
[https://doi.org/10.7736/KSPE.2013.30.2.236]

-
Choi, J. H. and Kim, G. M., “Development of an Air-Knife System for Highly Reproducible Fabrication of Polydimethylsiloxane Microstencils,” Journal of Micromechanics and Microengineering, Vol. 25, No. 8, Paper No. 085014, 2015.
[https://doi.org/10.1088/0960-1317/25/8/085014]

-
No, K. Y., Kim, G. D., and Kim, G. M., “Fabrication of Suspended Micro-Structures Using Diffsuser Lithography on Negative Photoresist,” Journal of Mechanical Science and Technology, Vol. 22, No. 9, pp. 1765-1771, 2008.
[https://doi.org/10.1007/s12206-008-0601-8]

-
Lee, J.-H., Choi, W.-S., Lee, K.-H., and Yoon, J.-B., “A Simple and Effective Fabrication Method for Various 3D Microstructures: Backside 3D Diffuser Lithography,” Journal of Micromechanics and Microengineering, Vol. 18, No. 12, Paper No. 125015, 2008.
[https://doi.org/10.1088/0960-1317/18/12/125015]

-
Sakai, Y., Yoshiura, Y., and Nakazawa, K., “Embryoid Body Culture of Mouse Embryonic Stem Cells Using Microwell and Micropatterned Chips,” Journal of Bioscience and Bioengineering, Vol. 111, No. 1, pp. 85-91, 2011.
[https://doi.org/10.1016/j.jbiosc.2010.08.014]