공압식 미세밸브를 이용한 다중유체 배열장치 개발
Copyright © The Korean Society for Precision Engineering
This is an Open-Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
We present a multi-sample array device based on a pneumatic system. Solenoid valves were used to control a micro valve in a pneumatic system. The use of a compressor together with a vacuum pump ensured that one outlet could supply both compression and vacuum pressure. The multi-sample array device was fabricated using conventional photolithography and PDMS casting. The device was composed of a multiplexer, sample array, and rinsing. The multiplexer could control four sample solutions injecting into the sample array chamber. Sample solution not arrayed was removed by DI-water from the rinsing inlet. To prevent trapping of microbubbles in the channel during injection of sample solution into the device, surfactant was added in PDMS solution to serve as a hydrophilic surface treatment. As a result, the device could be used as a sample array for 64 cases, using four samples and three columns of three chambers.
Keywords:
Sample array, Microfluidic system, Pneumatic system, Solenoid valve키워드:
샘플 배열, 미세유체시스템, 공압시스템, 솔레노이드 밸브1. 서론
미세유체시스템 (Microfluidic System)은 소량의 시약으로 신속한 합성, 분리, 정밀한 분석이 가능하다는 장점이 있기 때문에 생물학, 의학, 약학, 등 다양한 분야에서 적극적으로 연구되고 있다.1-4 샘플배열 (Sample Array) 기술은 미세유체시스템의 대표적인 분야로써 단시간 내에 샘플의 다양한 배열 및 조합이 가능하여 약물테스트, 세포독성테스트 등에서 다양하게 활용되고 있다.5,6 PDMS (Polydimethylsiloxane)는 인체 무해하며, 저렴한 비용과 높은 생산성뿐만 아니라 무독성, 기체 투과성, 탄성 등 다양한 장점을 가지고 있기 때문에 현재 PDMS기반의 미세유체장치를 이용한 다양한 연구가 진행되고 있다.7
미세유체장치를 이용한 샘플배열은 극소량의 유체를 정해진 위치에 배열하는 방식이다. 미세유체장치를 이용하여 샘플을 배열하기 위한 기존 방법은 두 가지의 액체가 혼합되지 않는 특성을 이용하여 액적을 제조한 후, 기하학적인 구조를 이용하여 채널 내부에서 원하는 위치에 배열시키는 방식이 있다.5,6 하지만 이러한 방식은 혼합되지 않는 두 가지 유체들이 주입되어야 하며 유체의 특성에 따른 미세유체칩 내부의 표면처리가 요구된다. 배열된 샘플은 특정크기 이상의 생성 및 유지가 어렵고, 모든 샘플이 채널로 연결되어 있어 샘플간의 간섭을 받기 때문에 다양한 변수 및 조건에 따른 유동을 최적화 해야 하는 어려움이 있다.8
반면 마이크로 밸브를 이용하면 유체 유동을 직접으로 제어할 수 있기 때문에 이러한 문제를 해결할 수 있다. 그래서 초소형 밸브구조의 제작이 필요하며, 특히 공압으로 작동하는 PDMS 기반의 마이크로 밸브에 대한 연구가 진행되고 있다.8-11 PDMS 기반의 마이크로 밸브는 PDMS의 탄성 및 복원력을 이용하여 유체의 구간을 연결 및 차단하는 방식을 가진다.11 마이크로 밸브는 크게 상시 개방형 밸브 (Normally Open Valve)와 상시 폐쇄형 밸브 (Normally Close Valve)로 나눌 수 있다. 상시 개방형 밸브는 압력이 없을 경우 개방되어 있는 형태로 유지되며, 압력이 작용할 경우 PDMS 박막이 변형되어 채널상의 유체의 흐름을 막아주는 방식이다.12,13 공기 채널내부에 정압을 가해지게 되면 PDMS 박막이 변형을 일으키면서 유체 채널 내부를 막게 된다. 그러나 이러한 방식은 유체를 지속적으로 막기 위하여 일정한 정압이 유지되어야 하며, 압력이 충분하지 못한 경우 마이크로 밸브로서의 기능을 제대로 수행할 수 없다. 이에 반해 상시 폐쇄형 밸브는 압력이 작용하지 않을 경우 PDMS 박막으로 유체가 차단된 상태에서 흡압을 이용하여 박막을 들어올려 유체채널을 개방하는 방식이다.14 상시 개방형 밸브와 비교하였을 때, 상시 폐쇄형 밸브는 제작과정 중 유체채널층과 PDMS 박막이 붙어있지만 접착이 되면 안되기 때문에 제작 과정이 상시 개방형 밸브보다 까다로우나, 마이크로 밸브 자체의 성능이 우수하여 다양한 디자인에 제작되고 있으며, 그 응용 또한 많이 소개되고 있다.15-17
본 연구에서는 공압시스템을 이용하여 상시 폐쇄형 마이크로 밸브가 포함된 능동적으로 여러 가지 유체 배열이 가능한 다중 유체 배열장치를 개발하고자 하였다. 진공펌프와 컴프레서를 연결하여 8개의 채널마다 흡압과 정압을 독립적으로 제어할 수 있도록 설계하였으며, 멀티플렉서를 이용한 4가지의 유체조합과 3개의 챔버를 이용하여 64가지의 유체배열을 구현할 수 있도록 하였다. 그리고 세척부를 추가하여 유체의 배열 후, 배열되지 않은 잔류 유체를 제거하여, 후처리공정이 보다 원활하게 진행될 수 있도록 설계하였다.
2. 실험방법
2.1 다중유체 배열장치의 설계 및 구상
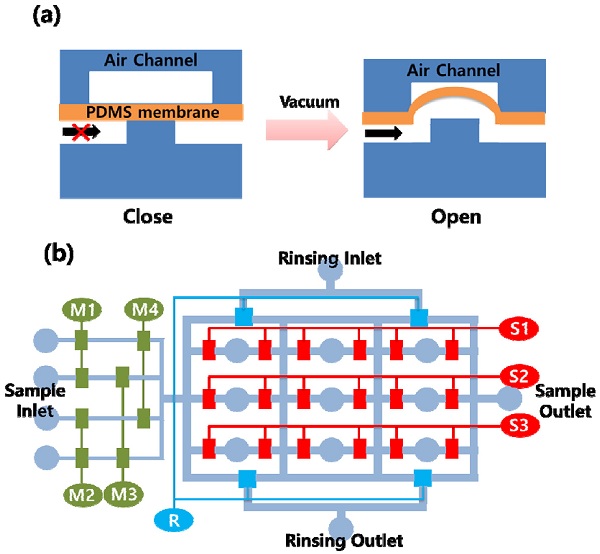
Fig. 1은 다중유체 배열장치에서 사용된 상시폐쇄형 밸브와 시스템의 전반적인 구성을 보여주는 개략도이다. 다중유체 배열 장치는 멀티플렉서부, 샘플배열부 그리고 세척부 등 세가지로 구성된다. 유체 샘플은 멀티플렉서를 통하여 선택적으로 주입되며, 미세채널을 통하여 샘플배열부로 이동하게 된다. 주입된 유체는 마이크로 챔버에 채워진 후 마이크로 밸브가 닫히며 배열된다. 샘플배열부에 배열되지 않은 잔류 유체들은 세척부에서 주입되는 탈이온수에 의하여 씻겨져 나가게 된다. 마이크로 밸브는 특정 외력이 마이크로 밸브에 작용하지 않을 경우 PDMS 박막에 의해 유체의 이동이 차단되며, 공기 채널에서 주입되는 흡합을 이용하여 PDMS 막을 위로 올려 아래층의 유체들이 흘러갈 수 있도록 한다. 다중유체 배열장치의 구성은 유체를 주입하는 멀티플렉서, 사용되는 마이크로 밸브는 멀티플렉서의 유체 주입을 위하여 4개(M1, M2, M3, M4), 챔버의 경우 3개(S1, S2, S3), 세척부에서 1개(R)로 전체 8개의 밸브들이 사용되며 세척을 위한 탈이온수의 주입을 위하여 1개의 실린지펌프 (Pump 11 Elite & Pico Plus, Harvard Apparatus, USA)가 사용된다. 멀티플렉서의 채널폭은 100 μm이며, 채널들이 모여서 샘플배열부로 넘어가는 부분은 200 μm로 제작하여 유체저항을 감소시켜 출구부분으로 역류하는 현상을 방지한다. M1-M4의 밸브를 이용하여 4가지의 유체들이 독립적으로 샘플배열부에 주입시킬 수 있다. 멀티플렉서를 통하여 주입된 4가지의 유체들이 3개의 챔버가 있는 3행의 채널들로 주입되며, 독립적인 제어가 가능하기 때문에 64가지 유체배열이 가능하다. S1-S3의 밸브들을 이용하여 마이크로 챔버상의 유체의 출입을 제어할 수 있다. 샘플을 배열하고 남아 있는 잔류샘플들은 R의 밸브를 이용하여 제거한다.
2.2 다중유체 배열장치의 제작
다중유체 배열장치 제작에 사용될 공기채널과 유체채널의 마스터몰드는 포토리소그라피 공정을 이용하여 제작된다. 감광제인 SU-8(2050)을 실리콘 웨이퍼 위에 붓고, 스핀코터를 이용하여 30초 동안 3000 RPM의 속도로 실리콘 웨이퍼 위에 고르게 도포한다. 65°C에서 30초, 95°C에서 6분의 소프트베이킹 공정을 이용하여 감광제상의 잔류 용매를 제거한 후 상온에서 서서히 냉각한다. 마이크로 패턴이 새겨진 마스크를 자외선 노광기에 설치한 후 도포된 실리콘 웨이퍼를 위치시킨다. 160 mJ/cm2만큼의 광량을 노광시켜 선택적으로 경화하여 마이크로 패턴을 제작한다. 그 후, 65°C에서 1분, 95°C에서 6분 동안 포스트 익스포져베이킹 공정을 이용하여 경화된 마이크로 패턴과 실리콘 웨이퍼의 사이의 점착력을 강화시킨다. SU-8 전용 현상액에 패턴이 형성된 실리콘 웨이퍼를 5분동안 담가 경화되지 않은 감광제를 제거한다. 질소가스와 IPA (Isopropyl Alcohol)로 세척 후, 마이크로 패턴의 표면 처리를 위하여 실렌나이즈처리 (Silanization)를 진행한다.
다중유체 배열장치의 유체채널과 공기채널은 앞선 과정을 통하여 제작된 마스터몰드 위에 PDMS 캐스팅 공정을 이용하여 제작된다. PDMS 엘라스토머와 경화제를 10:1 비율로 배합하여, 제작된 마스터 몰드 위에 붓고 진공펌프를 이용하여 배합중 발생한 거품을 제거한다.
유체 채널은 유체 주입 시 미세기포가 채널 안에 갇히는 현상을 방지하기 위하여 1wt.% 친수성 계면활성제 (Silwet L-77, Helena Chemical, USA)을 PDMS 용액에 첨가하여 배합하여 친수성 처리를 한다. 경화된 PDMS 블록은 마스터몰드에서 분리한 후 적당한 크기로 잘라 제작한다.
PDMS 박막을 제작하기 위하여 먼저 적당한 크기의 PET (Polyethylene Terephthalate) Sheet를 준비한다. PDMS와의 분리를 용이하게 하기 위하여 PET Sheet의 표면에 실렌나이즈 처리를 한다. PET Sheet를 스핀코터에 고정시킨 후 그 위에 PDMS 용액을 붓고 30초동안 3000 RPM의 속도로 고르게 도포한다. PDMS 용액이 도포된 PET sheet는 95°C의 오븐에서 30분가량 경화하여 제작한다.
앞선 과정을 통하여 제작된 공기채널과 PDMS 박막은 플라즈마 처리를 이용하여 결합하고 타공기를 이용하여 출구와 입구의 구멍을 뚫어준다. 결합된 공기 채널과 유체채널은 현미경을 이용하여 정렬하여 PDMS의 자체접착력으로 결합한다. 또한 내부에서 발생하는 압력으로 인한 누수현상을 막기 위하여 자체적으로 설계한 지그를 통하여 강도를 보강하여 다중유체 배열장치를 제작한다.
2.3 공압시스템 제작
공압시스템을 제작하기 위하여 솔레노이드 밸브에 PCB 기판을 이용하여 전원공급기와 스위치를 연결한다. Fig. 2는 제작된 공압장치와 공압시스템을 보여주는 사진이다. 공압시스템에는 8개의 솔레노이드 밸브 (PISCO sol V/V YSV10-DP-L, PSM, Korea)를 장착되어있다. 정압과 흡압을 독립적으로 제어하기 위하여 2개의 스위치를 설치하였다. 정압과 흡압을 위하여 두개의 입구를 가지고 있으나 하나의 출구를 가지기 때문에 동시에 사용할 수 는 없다.
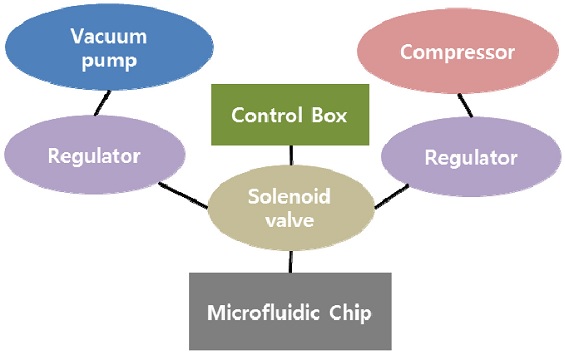
Fig. 3은 공압시스템의 구성도를 보여주는 개략도이다. 적정 정압과 흡압은 컴프레셔 (KAC-10S, KEYANG, Korea)와 진공펌프 (GAST DOA-P704-AC, GAST, USA)에 컴프레셔 레귤레이터 (TPC PR2, TPC Mechatronics Corp., USA)와 진공펌프 레귤레이터 (PISCO RVV 6UV, PSM, Korea)를 각각 연결하여 조절하였다. 압력을 조절하기 위한 레귤레이터들은 솔레노이드 밸브에서 연결되어 있으며, 솔레노이드 밸브는 컨트롤박스를 통하여 제어되며, 다중유체 배열장치에 흡압과 정압을 제공한다.
2.4 멀티액적 배열 장치와 공압시스템의 결합
상시 폐쇄형 밸브는 흡압을 발생하였을 때 닫혔던 PDMS 박막을 공기채널쪽으로 들어올려 유체를 지나가게 하는 방식이다. 그래서 유체채널과 PDMS 박막은 자체접착력만으로 결합하여야 한다. 그러나 내부의 압력을 지탱해줄 수 있는 지지체 없이 자체 접착력만으로 결합하게 되면, 내부의 압력이 증가하면서 유체가 새는 현상이 발생하였다. 이러한 문제를 해결하기 위하여 멀티샘플배열장치를 안정적인 작동을 위하여 강도를 보강할 수 있는 지그를 제작하였다 (Fig. 4(a)). 그리고 멀티플렉서부나 세척부에서 주입되는 액체를 보관하기 위하여 플라스틱 튜브를 이용하여 주입장치를 제작하여 샘플의 보관 및 주입이 용이하게 하였다(Fig. 4(b)). Figs. 4(c)와 4(d)는 유체가 주입되고 있는 다중유체 배열장치와 미세유체장치와 연결된 공압시스템의 전반적인 모습을 보여주는 사진이다.
3. 결과 및 고찰
3.1 멀티플렉서
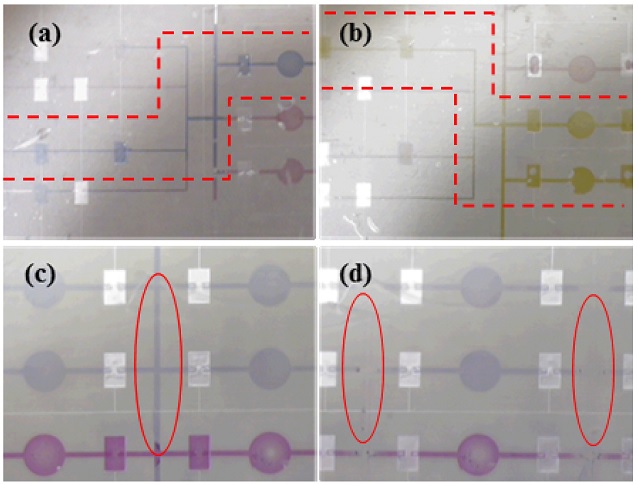
Figs. 5(a)와 5(b)는 멀티플렉서를 통하여 다양한 유체가 다중유체 배열장치에 들어가는 것을 보여주는 사진들이다. 모든 입구 부분에서 유체가 안정적으로 공급되는 것을 확인하였다. 공기채널의 폭이 100 μm일 경우 마이크로 밸브는 정상적으로 작동하였으나, 유체가 유체채널과 PDMS 박막 사이로 스며들어 다른 유체채널로 넘어가는 현상이 발생하였다. PDMS 박막과 공기채널의 폭의 비율이 1:1일 경우 유체가 박막 사이로 새지 않는 것을 확인하였으며, 공기채널의 폭이 50 μm, 박막이 30 - 50 μm일때 마이크로 밸브가 안정적으로 작동하였다. 유체를 다중유체 배열장치에 주입하였을 때, 압력이 15 kPa를 유지하였다. 그리고 마이크로 밸브를 제어하는 압력은 흡압이 30 kPa, 정압은 50 kPa를 유지하였다. 정압이 흡압보다 높은 이유는 상시 폐쇄형 밸브는 정압을 통하여 PDMS 박막을 눌러서 유체를 막는 방식으로 정압이 부족하게 되면 유체가 막히지 못하고 새는 현상이 발생하기 때문이다.
3.2 다중 유체 배열 및 세척
멀티플렉서에서 선택된 유체들이 세 가지의 독립적인 챔버에 성공적으로 배열되는 것을 확인하였으며 3개의 마이크로 밸브를 이용하여 독립적으로 제어할 수 있었다. 또한 Fig. 5(c)와 같이 샘플을 배열한 후 잔류 유체들은 채널 내부에 존재하게 되는데, 세척부에서 주입되는 1 ml/h의 탈이온수을 주입하여 세척하였다(Fig. 5(d)). 계면활성제를 PDMS 용액에 첨가하지 않았을 경우, Fig. 6(a)와 같이 샘플배열부에서 미세기포들이 빠져나가지 못하고 갇혀있는 것을 볼 수 있었다. 대조적으로 계면활성제가 첨가되었을 경우, 개질된 친수성 표면으로 인하여 미세기포들이 모두 빠져나가는 것을 확인할 수 있었다 (Fig. 6(b)). Figs. 6(c)와 6(d)는 계면활성제의 첨가 유무가 물과 PDMS 블록의 젖음성에 미치는 영향을 알아본 실험 사진들이다. 계면활성제를 첨가하지 않았을 경우, PDMS 블록와 물의 접촉각은 95°로 본래의 특성인 소수성을 나타낸 반면, 계면활성제를 첨가하였을 경우 접촉각이 66°로 친수성 표면을 가지게 되었다. 계면활성제가 포함된 PDMS에서 친수성 효과가 서서히 나타나기 때문에 1분 가량 지속적으로 유체를 주입하여 미세기포들이 제거하였다. 계면활성제의 첨가를 이용한 PDMS 친수성 처리방법은 수용성 유체의 다양한 실험 중 발생하는 미세기포 문제 해결에 많은 도움이 될 것으로 생각된다. 또한 이러한 표면 개질 방법은 여러 분야에서 목적에 따라서 다양하게 사용될 수 있다.
4. 결론
본 연구에서는 공압시스템을 제작하고 마이크로 밸브를 설계 및 제작하여 다양한 유체샘플의 배열이 가능한 다중유체 배열장치를 제작하였다. 공압시스템은 진공펌프와 컴프레서를 이용하여 정압과 흡압을 공급하며, 솔레노이드 밸브를 이용하여 제어할 수 있었다. 다중유체 배열장치는 포토리소그라피 공정과 PDMS 캐스팅 공정을 이용하여 제작하였다. 또한 친수성 계면활성제를 이용한 PDMS의 표면 개질을 통하여 채널상에 미세거품이 갇히는 현상을 해결할 수 있었다. 설계된 다중유체 배열장치는 마이크로 밸브를 이용하여 4개의 Inlet과 3개의 채널에서 총 64가지의 서로 다른 샘플배열이 가능하며 유체의 교환 역시 간단한 조작으로 수행할 수 있다. 그리고 다양한 장치와의 연계 및 조합이 가능하며 간단한 스위치 조작으로 누구나 쉽게 접근할 수 있으므로 세포배양을 위한 미세환경 조성 및 다양한 물질에 대한 세포 독성 테스트 등 액체샘플 기반의 실험을 위한 미세유체플랫 폼으로써 여러 분야에서 활용될 수 있을 것으로 예상한다.
Acknowledgments
본 연구는 미래창조과학부의 재원으로 한국연구재단의 지원(NRF-2012M3A9C6050112, NRF-2013R1A1A2060944)을 받아 수행되었음.
REFERENCES
-
Kim, H. G., Kim, K. M., Kim, Y. H., Lee, S. H., and Kim, G. M., “Preparation of Monodisperse ENX-Loaded PLGA Microspheres Using a Microfluidic Flow-Focusing Device,” Journal of Biobased Materials and Bioenergy, Vol. 7, No. 1, pp. 108-114, 2013.
[https://doi.org/10.1166/jbmb.2013.1263]

-
Kim, C. M., Park, S. J., and Kim, G. M., “Applications of PLGA Microcarriers Prepared Using Geometrically Passive Breakup on Microfluidic Chip,” Int. J. Precis. Eng. Manuf., Vol. 16, No. 11, pp. 2545-2551, 2015.
[https://doi.org/10.1007/s12541-015-0326-4]

-
Dang, T.-D., Kim, Y. H., Kim, H. G., and Kim, G. M., “Preparation of Monodisperse PEG Hydrogel Microparticles Using a Microfluidic Flow-Focusing Device,” Journal of Industrial and Engineering Chemistry, Vol. 18, No. 4, pp. 1308-1313, 2012.
[https://doi.org/10.1016/j.jiec.2012.01.028]

-
Choi, J. H. and Kim, G. M., “Micro-Patterning on Non-Planar Surface Using Flexible Microstencil,” Int. J. Precis. Eng. Manuf., Vol. 12, No. 1, pp. 165-168, 2011.
[https://doi.org/10.1007/s12541-011-0023-x]

-
Huebner, A., Bratton, D., Whyte, G., Yang, M., Abell, C., et al., “Static Microdroplet Arrays: a Microfluidic Device for Droplet Trapping Incubation and Release for Enzymatic and Cell-Based Assays,” Lab on a Chip, Vol. 9, No. 5, pp. 692-698, 2009.
[https://doi.org/10.1039/B813709A]

-
Cohen, D. E., Schneider, T., Wang, M., and Chiu, D. T., “Self-Digitization of Sample Volumes,” Analytical Chemistry, Vol. 82. No. 13, pp. 5707-5717, 2010.
[https://doi.org/10.1021/ac100713u]

-
Xia, Y. and Whitesides, G. M., “Soft Lithography,” Annual Review of Materials Science, Vol. 28 No. 1, pp. 153-184, 1998.
[https://doi.org/10.1146/annurev.matsci.28.1.153]

-
Kim, J., Taylor, D., Agrawal, N., Wang, H., Kim, H., et al., “A Programmable Microfluidic Cell Array for Combinatorial Drug Screening,” Lab on a Chip, Vol. 12, No. 10, pp. 1813-1822, 2012.
[https://doi.org/10.1039/c2lc21202a]

-
Unger, M. A., Chou, H. P., Thorsen, T., Scherer, A., and Quake, S. R., “Monolithic Microfabricated Valves and Pumps by Multilayer Soft Lithography,” Science, Vol. 288, No. 5463, pp. 113-116, 2000.
[https://doi.org/10.1126/science.288.5463.113]

-
Sundararajan, N., Kim, D., and Berlin, A. A., “Microfluidic Operations Using Deformable Polymer Membranes Fabricated by Single Layer Soft Lithography,” Lab on a Chip, Vol. 5, No. 3, pp. 350-354, 2005.
[https://doi.org/10.1039/b500792p]

-
Li, N., Sip, C., and Folch, A., “Microfluidic Chips Controlled with Elastomeric Microvalve Arrays,” Journal of Visualized Experiments: JoVE, Vol. 8, 2007.
[https://doi.org/10.3791/296]

-
Huang, S., He, Q., Hu, X., and Chen, H., “Fabrication of Micro Pneumatic Valves with Double-Layer Elastic Poly (Dimethylsiloxane) Membranes in Rigid Poly (Methyl Methacrylate) Microfluidic Chips,” Journal of Micromechanics and Microengineering, Vol. 22, No. 8, Paper No. 085008, 2012.
[https://doi.org/10.1088/0960-1317/22/8/085008]

-
Dy, A. J., Cosmanescu, A., Sluka, J., Glazier, J. A., Stupack, D., et al., “Fabricating Microfluidic Valve Master Molds in SU-8 Photoresist,” Journal of Micromechanics and Microengineering, Vol. 24, No. 5, Paper No. 057001, 2014.
[https://doi.org/10.1088/0960-1317/24/5/057001]

-
Au, A. K., Lai, H., Utela, B. R., and Folch, A., “Microvalves and Micropumps for BioMEMS,” Micromachines, Vol. 2, No. 2, pp. 179-220, 2011.
[https://doi.org/10.3390/mi2020179]

-
Hosokawa, K. and Maeda, R., “A Pneumatically-Actuated Three-Way Microvalve Fabricated with Polydimethylsiloxane Using the Membrane Transfer Technique,” Journal of Micromechanics and Microengineering, Vol. 10, No. 3, pp. 415-420, 2000.
[https://doi.org/10.1088/0960-1317/10/3/317]

-
Cooksey, G. A., Sip, C. G., and Folch, A., “A Multi-Purpose Microfluidic Perfusion System with Combinatorial Choice of Inputs, Mixtures, Gradient Patterns, and Flow Rates,” Lab on a Chip, Vol. 9, No. 3, pp. 417-426, 2009.
[https://doi.org/10.1039/B806803H]

-
Yang, W., Nam, Y. G., Lee, B. K., Han, K., Kwon, T. H., et al., “Fabrication of a Hydrophilic Poly (Dimethylsiloxane) Microporous Structure and Its Application to Portable Microfluidic Pump,” Japanese Journal of Applied Physics, Vol. 49, No. 6S, 2010.
[https://doi.org/10.1143/JJAP.49.06GM01]