미세섬유 기반의 생체적합성 관구조에 대한 기계적 물성 조절에 관한 연구
Copyright © The Korean Society for Precision Engineering
This is an Open-Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
There are various conduit structures such as arteries, veins, and airways in the human body, and they play critical roles in each tissue/organ. However, in recent years, the demand for artificial substitutes for the damaged conduit structure-based tissues and organs has significantly increased as dietary life has rapidly changed. Accordingly, various studies have been conducted, to develop a conduit structure of biocompatible polymers. In this study a 5 mm-diameter conduit structure was developed, using electrospinning process. An electrospinning setup equipped with a cylindrical-rod collector was constructed to fabricate a fibrous conduit structure, and then the impacts of process conditions on morphological and mechanical properties were investigated. Finally, it was shown that the mechanical properties of the fibrous conduit structure in circumferential direction, can be controlled by the electrospinning process conditions.
Keywords:
Electrospinning, Fibers, Conduit, Polycaprolactone키워드:
전기방사, 섬유, 관, 폴리카프로락톤1. 서론
최근 의료기술과 고분자 생체재료 기술의 발전에 힘입어 도관구조의 생체재료를 이용한 치료법이 활발하게 개발되고 있다. 이러한 치료에 사용되는 대표적인 관형 구조 생체재료로 인공혈관과 신경도관(Nerve Guide Conduit)이 있다. 우선 인공혈관은 기존의 혈관이식술에서 수급의 한계를 가진 자가유래 및 동종유래의 이식혈관을 대체하기 위한 것이며, 최근의 고령인구 증가 및 식습관 변화에 따라 혈관질환이 크게 증가하여 그 중요성이 더욱 커지고 있다[1]. 한편, 각종 외상, 부종 및 혈종에 의한 압박 등으로 신경이 손상될 경우 신경도관 이식을 통한 신경재생 치료가 이뤄지고 있다[2,3].
현재까지 성공적으로 개발되어 사용되고 있는 인공혈관은 5 mm 이상의 대구경이며 비분해성 소재로 만들어진 다공성의 관형태를 가진다[1]. 한 개발 예로 Nakagawa 등은 편물(Knitting)된 폴리에스터로 보강된 폴리우레탄 인공혈관을 개발하였다[4]. 또한 다양한 생체적합성의 분해성 소재를 이용한 인공혈관의 개발이 이뤄지고 있다. Mooney 등은 염침출된 PLGA (Poly Lactic-Co-Glycolic Acid) 필름을 말아서 도관조직의 지지체로 사용하였다[5]. Choi 등은 PGA (Poly (Glycolic Acid))와 PLCL (Poly (Lactide-Co-Ε-Caprolactone))를 염침출법 기반 용액주조(Solvent Casting) 방법을 이용하여 관형 구조 지지체로 제작하고, 동물실험을 통해 인공혈관으로의 활용 가능성을 보인 바 있다[6]. Kim 등은 에탄올을 이용한 딥코팅 공정을 통해 유연성을 가진 분기형 인공혈관을 제작하였다[7]. 그 외에도 다양한 인공혈관 제작 방법들이 연구되고 있다[8,9].
신경도관에 대한 연구도 활발히 진행되고 있다. 이는 관구조 지지체를 이용하여 신경세포 재생을 유도하는 것을 기반으로 하고 있다. Lee 등은 고어택스(Gore-Tex) 기반 관구조가 신경도관으로 사용될 수 있음을 보였다[10]. Jeong 등은 얼읍입자 동결건조법을 이용하여 탈미네랄화된 골분을 포함한 PLGA 관구조를 제작하여 척수신경을 재생한 연구를 수행하였다[2]. Cho는 분기형 봉구조 탬플릿에 PCL (Polycaprolactone), PEO (Polyethylene Oxide) 소재의 섬유를 둘러말고 어닐링(Annealing)한 후 PEO를 침출시키는 방법으로 다공성/비다공성의 이중구조를 가지는 신경도관 구조를 제작하였다[3].
이러한 방법들과 함께 대표적인 인공혈관 및 신경도관 제조 방법으로 전기방사(Electrospinning) 공정이 있으며, 이 방법을 이용하여 다양한 인공혈관 및 신경도관용 관구조가 제작되었다[11-15]. 기존의 연구에서는 다양한 구조 및 소재 다변화를 통해 기계적 물성치 향상을 고려한 바 있다. 그러나 관 구조가 내부를 유동하는 유체의 압력으로 인해 원주 방향으로 팽창하는 점을 고려할 필요가 있음에도 불구하고, 전기방사 공정조건에 따른 관구조의 원주 방향에 대한 기계적 물성치 변화에 대한 연구는 찾기 어렵다. 이는 수 mm의 직경을 가지는 관구조에 대한 물성 측정[16] 및 공정조건 다변화에 어려움이 있기 때문으로 추정된다.
본 연구에서는 봉형의 회전 집적기(Collector)를 이용한 용액 기반 전기방사를 통해 섬유구조로 구성되어 다공성과 유연성을 가진 직경 5 mm의 관형 구조를 제작할 수 있음을 보였다. 특히 용액 토출유량(Flow Rate)과 집적기 회전속도 등의 전기방사 공정조건을 조절하여 섬유의 직경 및 정렬도 등의 섬유구조 특성들에 대한 영향을 확인하였다. 특히, 공정조건의 변경을 통해 원주 방향의 기계적 물성치를 조절할 수 있음을 보였다.
2. 미세섬유 도관구조의 제작
2.1 전기방사 장치의 구성
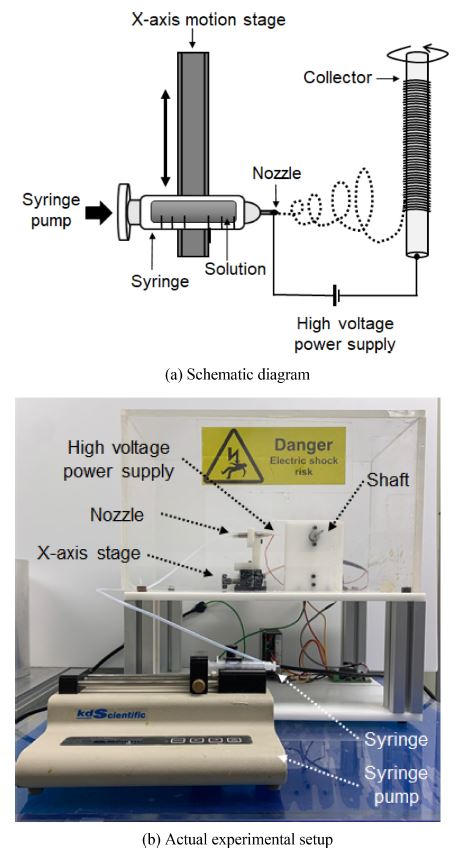
관 형상의 미세섬유 구조물 제작을 위해 전기방사 장치를 구성하였다. 관 형상의 미세섬유 구조물은 방사된 미세섬유를 회전하는 봉형의 집적기를 이용하여 제작할 수 있다. 따라서 본 연구에서 사용된 전기방사 장치는 주사기 펌프, 내경이 210 μm인 노즐(Nozzle), 폴리테트라플루오로에틸렌(Polytetrafluoroethylene) 튜브, DC 모터로 회전되는 스테인리스강 소재의 5 mm 직경을 가지는 봉형 집적기, 그리고 노즐과 집적기 사이에는 고전압 공급기를 이용하여 고전위를 부가하였다. 이때 노즐에는 양극을 그리고 집적기는 접지시켰다. 노즐은 직선 이송스테이지를 이용하여 집적기의 축 방향을 따라 왕복직선운동을 할 수 있도록 하였다. Fig. 1(a)는 본 연구에서 사용된 전기방사 장치를 보여준다. Fig. 1(b)에 보인 바와 같이 전기방사 장치는 아크릴 박스 내에 설치되어 외부와 분리되었다.
2.2 도관구조 제작 실험
본 연구에서 전기방사에 사용된 고분자는 평균분자량이 150,000인 펠렛(Pellet) 형태의 PCL (Sigma Aldrich Co.)이었으며, 용매는 클로로폼(Chloroform, Samchun Chemicals)이었다. PCL을 클로로폼에 8 wt%의 농도로 녹여 전기방사 용액을 준비하였다. 본 연구에서는 구조물의 기계적 물성을 조절하기 위해 용액의 토출유량과 집적기 회전속도를 조절하였으며, 그 외의 공정변수는 고정하였다. 전기방사 시의 주변 온도와 상대습도는 각각 20oC와 50%를 유지하였다. 노즐과 직접기 표면과의 거리(Tip-To-Collector Distance)와 전위차는 각각 70 mm와 10 kV이었다. 축방향의 70 mm 길이의 집적기에 섬유가 균일하게 감길 수 있도록 0.25 mm/min의 속도로 노즐을 왕복이송하였다. 실험에 사용된 용액의 토출유량 조건은 0.1, 0.3, 0.5 ml/h이며, 집적기 회전속도는 2,000, 3,000, 4,000 rpm이었다. 이상의 실험조건은 Table 1에 제시되어 있다.
전기방사된 관형의 미세섬유는 부직포와 같이 적층이 되어 있으므로 섬유 간 결합성을 개선하기 위해 어닐링을 수행하였다. 미세섬유는 집적기에 집적된 그대로 진공오븐(Jeio Tech Co.)을 이용하여 50oC의 온도에서 4시간 동안 어닐링되었다. 어닐링 후 미세섬유 관형 구조는 형태를 유지하며 집적기로부터 분리되었다. Fig. 2는 제작된 미세섬유 관형 구조를 보여준다. 이로부터 미세섬유 기반의 관형 구조가 성공적으로 제작되었음을 알 수 있다.
2.3 분석 방법
전자현미경을 이용하여 제작된 미세섬유 관형 구조의 형상분석을 수행하였다. 이를 위해 제작된 조건별 시료 5개에 팔라듐(Palladium)을 증착하고 전자현미경(Hitachi)으로부터 촬영된 이미지에 대해 ImageJ 소프트웨어(NIH)를 이용하여 섬유의 집적 형상과 직경을 반복 측정하였다.
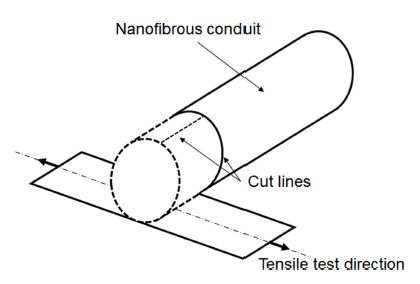
구조물의 기계적 물성을 측정하기 위해 만능재료시험기(Instron)를 이용하여 인장시험을 수행하였다. 특히, 관형 구조가 내부를 유동하는 유체의 압력으로 인해 팽창하는 점을 고려하여 원주 방향에 대한 응력-변형률 특성을 확인하였다. 이를 위해 Fig. 3에 보인 바와 같이 제작된 관형 구조를 폭 5 mm로 절단하고 다시 축 방향으로 한쪽을 잘라 5 × 15.7 mm2 크기의 조건별로 5개씩의 시료를 준비하고, 각 시료가 150% 인장까지 응력-변형률 거동을 확인하였다.
3. 미세섬유 관형 구조의 분석
3.1 토출유량에 따른 특성 분석
Fig. 4는 Table 1에 주어진 조건에서 집적기 회전속도를 3,000 rpm으로 유지한 상태에서 다양한 토출유량 조건으로 제작된 관형 구조의 미세섬유 형상을 보여준다. 그림으로부터 토출유량에 따라 전기방사된 PCL 섬유의 형상이 큰 차이를 가짐을 알 수 있다. 우선, 토출유량이 클수록 섬유 직경이 증가함을 확인할 수 있다. 또한 그림의 수직 방향이 관형 구조의 원주 방향임을 고려할 때 토출유량이 클수록 섬유의 정렬성도 증가하는 것을 알 수 있다.

PCL fibers electrospun under various flow rate conditions. Vertical direction in the images corresponds to circumferential direction of fiber conduit structure
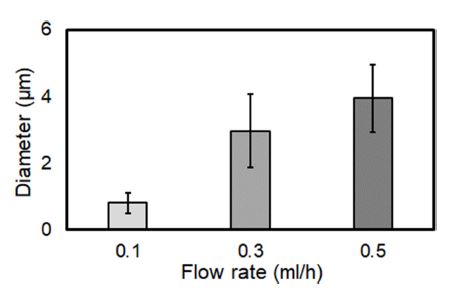
Fig. 5는 토출유량에 따른 섬유의 직경을 보여준다. 0.1 ml/h의 토출유량 조건에서 섬유 직경이 가장 작고 균일 하며 평균직경과 표준편차는 각각 0.887, 0.338 μm이었다. 한편, 0.3 mL/h의 토출유량 조건에서는 평균직경이 2.808, 표준편차는 1.141 μm로서 평균직경과 표준편차가 0.1 ml/h의 토출유량 조건에 비해 상당히 증가하였다. 토출유량이 0.5 mL/h일 때는 평균직경이 3.954, 표준편차가 1.083 μm로서 가장 컸다. Fig. 4의 그림에서도 보인 바와 같이 섬유의 직경은 토출유량이 증가할수록 크게 증가함을 볼 수 있으며, 이는 용액의 유량이 증가할수록 노즐 끝단에서의 섬유의 직경이 크고, 이로 인해 집적기에 다다르기 전까지 공기 중에서의 섬유의 휘핑(Whipping) 운동 또한 적어 섬유의 연신이 상대적으로 적고 단면적의 감소 또한 적어지기 때문이다.
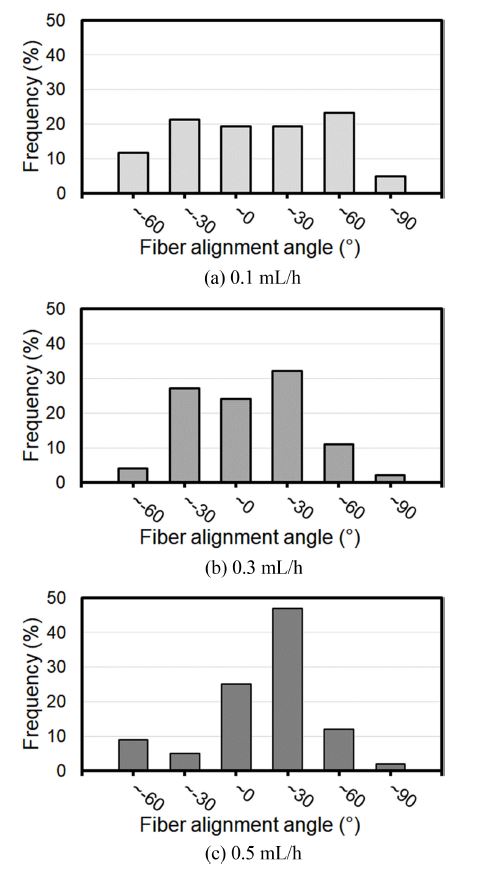
Fig. 6은 각 토출유량 조건에 따른 섬유의 집적 각도를 보여준다. 수직 방향을 0o로 하여 시계방향으로의 각도를 양의 값으로 할 때 각도의 분포를 확인할 수 있다. 그림으로부터 0.1 ml/h의 토출유량 조건에서는 -60부터 +90o까지 다양한 각도로 집적된 섬유가 고르게 존재하며, 이로부터 섬유의 집적에 있어서 특정한 방향성을 가지지 않는다고 평가할 수 있다. 그러나, 토출유량이 0.3 ml/h일 때는 그 분포가 0o 근처를 중심으로 분산 값이 줄어든 것을 알 수 있다. 이로부터 방향성이 향상된 것으로 평가할 수 있다. 0.5 ml/h의 조건에서도 이러한 경향이 두드러지게 커졌음을 알 수 있으며, Fig. 4의 그림과도 잘 부합한다. 이는 Fig. 5에서도 언급한 바와 같이 토출유량의 증가에 따라 섬유의 휘핑운동이 감소하고 이에 따른 연신도 줄어 집적기 표면에서의 섬유의 속도와 집적기 표면의 접선속도와의 차이가 상대적으로 줄기 때문으로 추정된다. 0.1, 0.3, 0.5 ml/h에서 각도 분포의 표준편차는 각각 42.8, 32.6, 32.5o이었다. 정렬도 측면에서 0.1 ml/h의 조건은 특별한 방향성을 가지지 않으므로 관형 구조의 원주 방향 물성조절 측면에서는 어려움이 있으며, 0.5 ml/h의 조건은 원주 방향으로의 방향성은 매우 높으나 길이방향(Longitudinal Direction)으로의 기계적 물성치 보장에는 어려움이 있다. 0.3 ml/h의 조건은 원주 방향과 그 외 방향으로의 방향성이 다른 조건에 비해 높아 주어진 조건 중 가장 적합한 것으로 판단하였다.
3.2 집적기 회전속도에 따른 특성 분석
토출유량이 0.3 ml/h일 때 원주 방향 기계적 물성을 조절하기 위해 집적기의 회전속도를 2,000, 3,000, 4,000 rpm로 하여 미세섬유 관형 구조를 제작하였다. Fig. 7은 2,000, 4,000 rpm의 집적기 회전속도일 때 제작된 관형 구조의 표면에 대한 SEM 이미지를 보여준다. 그림으로부터 섬유의 직경은 Fig. 4(b)와 비교적 유사하며, 회전속도의 변화에는 큰 영향을 받지 않았음을 알 수 있다. 정렬도는 육안을 이용한 구분이 어려움을 확인할 수 있다.
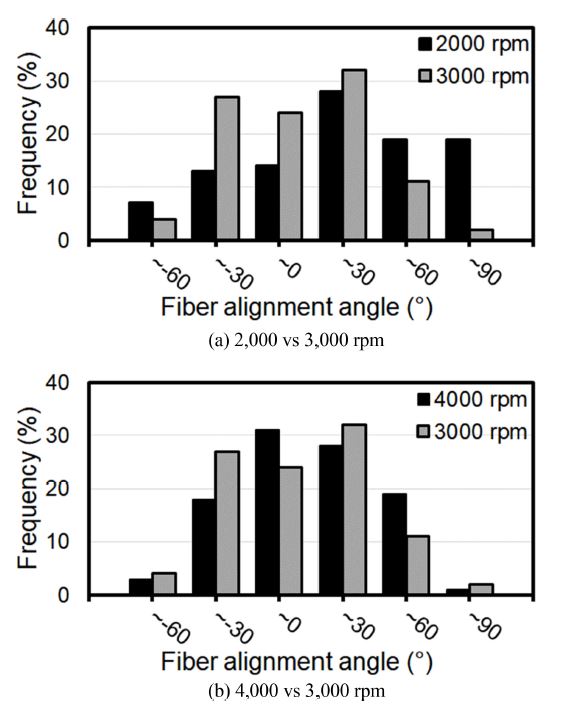
Figs. 8은 섬유의 정렬도에 대해 6(b)와 비교한 결과를 보여준다. Fig. 8(a)로부터 정렬각도의 분포 측면에서 2,000으로 전기 방사한 경우 3,000 rpm의 경우에 비해서는 60과 90o의 성분이 현저히 증가한 것을 볼 수 있어 정렬도가 낮음을 알 수 있다. Fig. 8(b)에서 4,000의 경우와 3,000 rpm의 경우 분포의 차이가 현저히 드러나지는 않으나, 0o 주변으로의 집중도가 개선되었음을 알 수 있다. 또한, 분포의 표준편차를 확인해보면, 2,000, 3,000, 4,000 rpm에서 표준편차는 각각 43.9, 40.6, 31.0o로 회전속도가 증가함에 따라 줄어들었다. 이로부터 회전속도 조절을 통해 정렬도를 조절할 수 있음을 확인하였다.
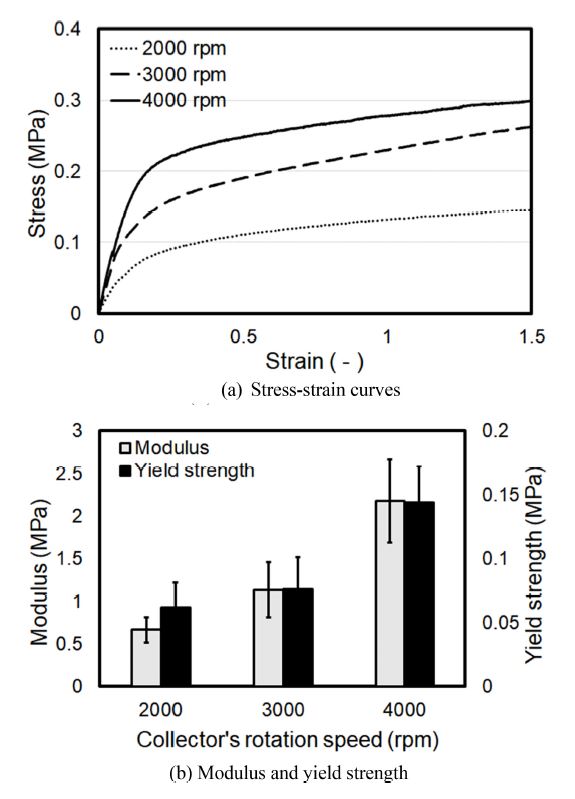
집적기의 회전속도 별로 제작된 미세섬유 관형 구조에 대해 Fig. 3에서 보인 바와 같이 시료를 준비하고 인장시험을 통해 얻어진 응력-변형률 선도를 Fig. 9(a)에서 보여준다. 그림으로부터 회전속도가 빠른 조건에서 얻어진 관형 구조일 수록 동일 변형률에 대해 높은 응력을 가짐을 볼 수 있다. 응력-변형률 선도로부터 고분자의 탄성률(Modulus)와 항복강도(Yield Strength)를 추출하였다. Fig. 9(b)는 초기 0.03의 변형률 이내에서의 탄성율과 0.2%-오프셋(Offset)법을 적용하여 추정된 고분자 항복응력을 보여준다. 이미 Fig. 9(a)에서도 제시된 바 있으나, 탄성율과 항복강도가 집적기의 회전속도에 따라 현저한 차이를 가짐을 알 수 있다. 특히 4,000 rpm 조건에서는 다른 두 조건에 비해 큰 폭의 증가가 있었다. 이로부터 집적기 회전속도를 증가시키면 원주 방향으로 섬유의 정렬도가 증가하여 기계적 물성을 개선할 수 있음을 알 수 있다.
4. 결론
본 연구에서는 신경도관과 인공혈관과 같이 의료 분야에서 높은 수요가 있는 다공성 생체적합성 고분자 소재의 관형 구조를 전기방사 공정을 이용하여 섬유구조로 제작하고, 관 구조의 중요한 기계적 물성치인 원주 방향에 대한 기계적 특성을 조절할 수 있음을 보였다. 제작을 위해 원형 봉 집적기를 포함한 전기방사장치를 구성하였다. 전기방사 공정에서 용액의 토출유량과 집적기의 회전속도를 조절하며 섬유의 직경과 정렬도를 조절할 수 있음을 보였다. 본 연구의 실험조건에서는 섬유의 직경을 약 900 nm에서 4 μm 범위에서 조절 가능하였으며, 정렬각도의 표준편차는 약 31.0-43.9o 범위에서 조절할 수 있음을 확인하였다. 특히 주어진 토출유량 조건에서 집적기의 회전속도를 조절함으로써 정렬각도의 분포 조절을 통해 관형 구조의 원주 방향 기계적 물성치를 조절할 수 있음을 실험적으로 확인하였다.
Acknowledgments
이 논문은 2022년도 정부(과학기술정보통신부)의 재원으로 한국연구재단 지원을 받아 수행된 연구임(Nos. NRF-2020R1A4A1018652, NRF-2021R1A2C2014364).
REFERENCES
- Lee, M. H., Park, H. K., Park, J. C., Park, K. D., Park, Y. H., (2007), Research for improving of artificial vascular graft, Biomaterials Research, 11(4), 156-161.
- Jung, S. H., Kim, S. H., Kim, C. M., Hong, H. H., Jeon, N. R., Kim, W., Lee, D., Rhee, J. M., Khang, G., (2009), Tissue engineered spinal cord using SC, OEC and BMSC seeded DBP/PLGA nerve channel; Preliminary study, Tissue Engineering and Regenerative Medicine, 6(4-11), 685-692.
-
Cho, Y. S., Fabrication of branched PCL nerve guide conduit with a dual structure using porous/biodegradable PCL filaments, Transactions of the Korean Society of Mechanical Engineers, B, 45(4), 205-210, 2021.
[https://doi.org/10.3795/KSME-B.2021.45.4.205]

-
Nakagawa, Y., Ota, K., Sato, Y., Teraoka, S., Agishi, T., (1995), Clinical trial of new polyurethane vascular grafts for hemodialysis: Compared with expanded polytetrafluoroethylene grafts, Artificial Organs, 19(12), 1227-1232.
[https://doi.org/10.1111/j.1525-1594.1995.tb02290.x]

-
Mooney, D., Organ, G., Vacanti, J., Langer, R., (1994), Design and fabrication of biodegradable polymer devices to engineer tubular tissues, Cell Transplantation, 3(2), 203-210.
[https://doi.org/10.1177/096368979400300209]

- Choi, J.-W., Lim, S.-H., Hong, Y.-S., Kim, B.-S., (2008), Development of artificial vessels with autologous bone marrow cells and polymers, Journal of Chest Surgery, 41(2), 160-169.
-
Kim, Y. S., Lee, S. M., Kim, Y. S., Yoo, D. H., Park, S.-H., (2021), A study on enhanced uniformity of artificial flexible vascular grafts fabricated by dip-coating process, Journal of the Korean Society for Precision Engineering, 38(5), 365-371.
[https://doi.org/10.7736/JKSPE.021.009]

-
Nemeno-Guanzon, J. G., Lee, S., Berg, J. R., Jo, Y. H., Yeo, J. E., Nam, B. M., Koh, Y.-G., Lee, J. I., (2012), Trends in tissue engineering for blood vessels, Journal of Biomedicine and Biotechnology, 2012.
[https://doi.org/10.1155/2012/956345]

-
Niklason, L. E., Langer, R. S., (1997), Advances in tissue engineering of blood vessels and other tissues, Transplant Immunology, 5(4), 303-306.
[https://doi.org/10.1016/S0966-3274(97)80013-5]

- Lee, K. H., Oh, S. H., Lee, S. R., Kang, N. H., (2005), The availability of Gore-Tex® tube as nerve conduit at the peripheral nerve defect, Archives of Plastic Surgery, 32(5), 613-618.
-
Moore, M. J., Tan, R. P., Yang, N., Rnjak-Kovacina, J., Wise, S. G., (2021), Bioengineering artificial blood vessels from natural materials, Trends in Biotechnology, 40(6), 693-707.
[https://doi.org/10.1016/j.tibtech.2021.11.003]

-
Awad, N. K., Niu, H., Ali, U., Morsi, Y. S., Lin, T., (2018), Electrospun fibrous scaffolds for small-diameter blood vessels: A review, Membranes, 8(1), 15.
[https://doi.org/10.3390/membranes8010015]

-
Niklason, L. E., Lawson, J. H., (2020), Bioengineered human blood vessels, Science, 370(6513), eaaw8682.
[https://doi.org/10.1126/science.aaw8682]

-
Vijayavenkataraman, S., (2020), Nerve guide conduits for peripheral nerve injury repair: A review on design, materials and fabrication methods, Acta Biomaterialia, 106, 54-69.
[https://doi.org/10.1016/j.actbio.2020.02.003]

-
Houshyar, S., Bhattacharyya, A., Shanks, R., (2019), Peripheral nerve conduit: Materials and structures, ACS Chemical Neuroscience, 10(8), 3349-3365.
[https://doi.org/10.1021/acschemneuro.9b00203]

-
Mi, H.-Y., Jiang, Y., Jing, X., Enriquez, E., Li, H., Li, Q., Turng, L.-S., (2019), Fabrication of triple-layered vascular grafts composed of silk fibers, polyacrylamide hydrogel, and polyurethane nanofibers with biomimetic mechanical properties, Materials Science and Engineering: C, 98, 241-249.
[https://doi.org/10.1016/j.msec.2018.12.126]


Post-Doctoral Research Fellow in Kyungpook National University. Her research interests are bioengineering and advanced manufacturing processes.
E-mail: jeonghk@knu.ac.kr

Senior Staff in the PI Advanced Materials.
E-mail: choijw0907@pimaterials.com

Chief Executive Officer (CEO) of ST1 Co., Ltd.. His research interest is electrospinning and nanofiber applications.
E-mail: yjyoon@artipore.com

Professor in School of Mechanical Engineering, Kyungpook National University. His research interest is advanced manufacturing processes.
E-mail: yhjeong@knu.ac.kr