회전자력 작용에 의한 이온 수송에 관한 실험적 연구
Copyright © The Korean Society for Precision Engineering
This is an Open-Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
Hydrogen production using water electrolysis is generally a well-known phenomenon. Hydrogen produced using the water electrolysis method is an environment-friendly energy source called ‘green hydrogen’ that does not emit any environmental pollutants when using renewable energy as an energy source. This study aims to improve the efficiency of hydrogen production by using the ion transportation effect induced by a rotating magnetic force. For this purpose, the experimental conditions for ion transport were determined through an experiment using a copper wire and the rotating magnetic force for water electrolysis was applied using an alkali aqueous solution. Based on the results, an increase in the number of bubbles generated by the rotating magnetic force increased was observed. It is assumed that the efficiency of hydrogen production using water electrolysis can be improved by the rotating magnetic force.
Keywords:
Magnetic field, Ion transportation, Magneto-hydrodynamics, Water electrolysis, Hydrogen키워드:
자기장, 이온 수송, 자기 유체역학, 수전해, 수소1. 서론
수소는 화석연료의 유한성과 온실가스 및 대기 오염물질 배출 문제가 없는 청정 에너지원으로서 미래 에너지원으로 여겨지고 있다. 수소 생산 기술은 원료에 따라 크게 화석연료의 개질법, 바이오매스 전환법, 수전해법으로 분류된다. 수소 생산방법 중 수전해는 높은 순도의 수소를 생산하는 가장 일반적인 방법이다. 수전해를 이용한 수소제조는 간편할 뿐만 아니라 에너지의 저장 및 수송이 쉽다.
수전해 기술은 사용되는 방법에 따라 고분자 전해질막 전기분해(PEM), 고온 전기분해(HTE) 및 알칼리성 전기분해(AE) 방법으로 나눌 수 있다. PEM 방식은 고체 고분자 전해질막을 이용한 수전해 방식이며, 고분자 전해질막은 발생된 가스를 분리하고 수소 이온이 양극에서 음극으로 이동하는 통로 역할을 한다. HTE 방식은 작동 온도가 증가함에 따라 수전해 반응에 필요한 자유 에너지가 감소하면서, 수전해에 필요한 전기량이 감소한다는 원리를 사용한다. HTE 수전해 방식은 고온 또는 고전류 밀도를 필요로 하며, 생산 설비를 축소 및 단순화하고 고순도 수소를 대량으로 얻을 수 있지만 내구성과 효율이 낮고 작업 시간이 짧다. Chauveau et al. [1]은 고온 증기 전기분해가 수소의 대량 생산을 위한 가장 유망한 방법 중 하나라고 보고하였다.
AE 방식은 높은 에너지 효율과 낮은 설치 비용을 보여 많은 연구가 진행되고 있다. 하지만 AE 방식은 알칼리성 전해질을 사용해야 하므로 다양한 안전상의 이유로 취급이 어렵고 금속 부식에 취약하다.
수소 생산 기술에서 효율성과 안전성 확보는 가장 중요한 요소로 여겨진다. 현재 AE 방식을 이용한 수소 생산 효율 향상을 위한 연구는 주로 전극과 촉매의 개발, 전해질의 종류와 농도에 관한 연구가 대부분이다. Nagai et al. [2], Kaninski et al. [3], and De Souza et al. [4,5]은 알칼리성 전해질(KOH, NaOH), 산성 전해질(HCl, H2SO4), 전극 간 거리, 유동 효과 및 용액 온도와 같은 작업 매개 변수가 물의 수소 생성 속도에 미치는 영향을 조사하였다. Nikoli et al. [6]은 알칼리 전해조를 사용하여 복합 형태의 이온 및 현장에서 활성화하는 화합물을 추가하여 보다 효율적으로 수소를 생성하였으며, 이 보고서에서 생성된 수소의 질량 단위당 에너지 필요량은 약 15% 감소했다. Licht et al. [7]은 교반에 의한 전해조의 흐름으로 인해 전극 표면 근처의 이온 농도가 증가할수록 전기분해 효율이 향상될 수 있음을 보여주었으며, Zhang et al. [8]은 수소 생산을 위한 물 전기분해시스템의 최적 설계에 대한 지침을 제공했다.
수소는 그 자체가 연료이자 매우 높은 효율로 전기를 생산할 수 있는 에너지원으로서 이차전지보다 훨씬 더 높은 에너지 밀도를 갖는 에너지 저장 매체이다. 수전해 기술을 이용한 수소 생산 시스템의 전해질에 대한 연구 결과에서 수산화칼륨(KOH)이 가장 효과적인 전해질로 평가되며[9], 30% 이상의 농도에서는 큰 차이가 없는 것으로 알려져 있다[10].
수소 이온 전도성 전해질의 구동 환경을 제어하여 ‘이온 활성화 전해질’을 구현하였으며, 기존 최고 효율의 수전해 장치에 비해 수소 생산 효율이 약 4배 높은 것으로 확인되었다[11]. 보고서에서 수소의 생산 효율은 전해질에서 이온의 확산 및 전도 속도에 따라 크게 달라질 수 있음을 알 수 있다.
물의 이론상 수전해 전압은 1.23 eV이나, 수전해 시스템에는 분리기, 전해조, 반응기 등으로 인해 이온의 흐름을 방해하는 저항이 있어 실제로는 더 높은 전압이 요구된다. 따라서 수전해의 경제성과 효율을 높이기 위해서는 저항을 낮추는 것이 가장 중요하다.
자력이 전자나 이온의 위치를 제어하는데 사용될 수 있다는 것은 잘 알려져 있다. 이 현상은 대부분의 발전소에서 전기를 생산하기 위해 사용되며, 이온가속기, 이온빔 등 다양한 분야에서 활용되고 있다. 자력이 화학 전기장에 미치는 영향에 대한 이전 연구의 대부분은 전기도금을 포함하며, 자력에 의한 로렌츠력이 전해액의 대류를 증가시키고 농도 분극과 옴 분극을 감소시켜 저전류 전기도금이 가능해진다. Matsushima et al. [12]은 구리도금 공정에 자력을 가함으로써 이온의 대류가 증가함을 확인하였으며, 자력에 의해 이온 농도 확산 속도와 전류 밀도가 증가하고 구리 표면의 증착 속도가 증가함을 확인하였다. Bund et al. [13]은 두 전극 사이의 전류 방향과 1T의 안정된 자력 방향을 이용하여 전류 밀도를 제한하는 실험을 수행하였다. 이 실험을 통해 자력의 영향으로 미세입자가 형성되는 경향이 있음을 확인하였다.
또한, 자력을 이용한 이온의 위치 제어와 관련된 몇몇 연구가 수행되었다. Yunet et al. [14]은 코로나 방전에 의해 발생하는 이온은 자력을 이용하여 가속할 수 있으며, 자석을 사용하지 않을 때보다 약 3배의 속도를 얻을 수 있다고 보고하였다. 또한 수전해와 관련하여 Iida et al. [15] 및 Hisayoshi et al. [16]은 자력 하에서 전극 사이의 거리와 전해질의 종류에 따른 수전해 실험을 수행하였다. 실험에 따르면 전극 사이의 거리가 짧을수록 용액의 농도가 낮고 자기력이 강할수록 자기력으로 인한 전압 차가 커진다는 것을 확인하였다.
따라서 자력에 의해 이온의 이동을 제어할 수 있고, 수전해 시스템의 저항이 낮아져 효율이 향상된 수전해 시스템을 개발할 수 있을 것으로 생각된다. 본 연구에서는 수전해 시스템 내부의 RMH의 회전을 통하여 자력의 발생 위치를 회전시켜 이온의 이동을 제어할 수 있는 수전해 시스템을 개발하고, 자력의 회전이 수소 생산에 미치는 영향을 확인하고자 하였다.
2. 실험
2.1 실험 장치
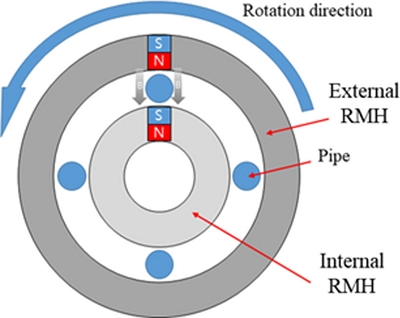
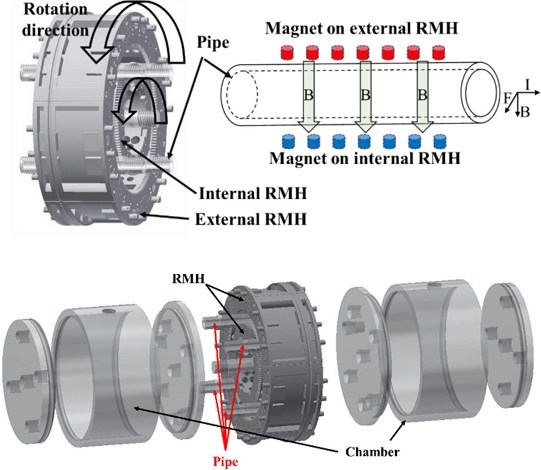
Fig. 1은 본 연구에서 고안한 실험 장치의 개념도를 나타낸다. 자석의 다른 극은 파이프에 자기장을 부여하기 위해 파이프의 내부와 외부에 배치되었다. Fig. 2에서 알 수 있듯이 실험 장비는 수용액을 가득 채울 수 있는 2개의 챔버, 챔버를 연결하는 4개의 파이프 및 Rotary Magnet Holder (RMH)로 크게 나눌 수 있다. RMH는 Figs. 1과 2에서 나타낸 것과 같이 내부 RMH와 외부 RMH로 구성된다.
2.2 Rotary Magnet Holder (RMH) 설계
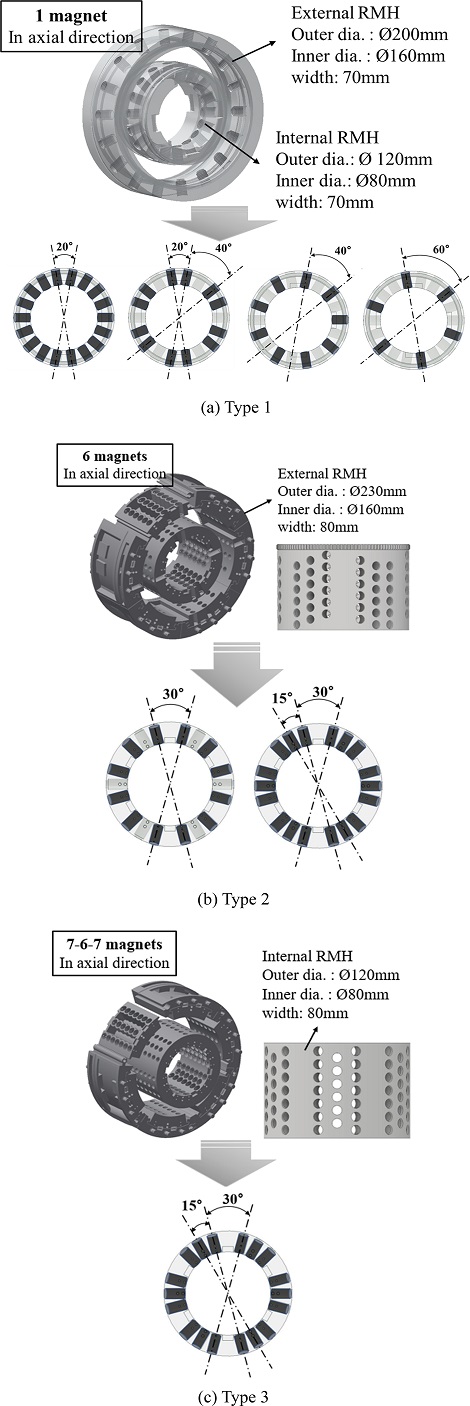
RMH Type 1은 Fig. 3(a)와 같이 1열의 자석은 원주 방향 20o 간격으로 배치할 수 있도록 하였으며, 내부 및 외부 RMH에 각각 18개씩 배치되도록 설계하였다. 또한, 자기장을 회전시키기 위해서 내부 및 외부 RMH는 벨트-폴리 시스템을 적용하여 동일한 속도로 회전하도록 제작되었다. 자석의 배치 간격은 20, 20/40, 40 및 60o 간격으로 선정하였으며, 이온 수송 효과를 확인하기 위해, 먼저 수용액 대신에 파이프에 구리 선을 관통시켜 코일을 형성하고, RMH의 회전속도에 따른 전압 신호를 측정하였다. RMH Type 2는 더 강한 자기력을 제공하기 위해 내부/외부 RMH에 파이프의 길이 방향으로 6열의 자석을 원주 방향으로 15/15/30o 간격으로 배치할 수 있도록 설계되었으며, 각 108개씩 총 216개의 자석을 배치할 수 있다. 이를 이용하여 Fig. 3(b)에 나타낸 것과 같이 30o 간격으로 자석을 배치하였다. RMH Type 2를 이용한 실험에서도 RMH Type 1과 마찬가지로 구리 선을 이용하여 자기장 회전 시 발생되는 전압 신호를 측정하였다. 이러한 RMH Type 1 및 Type 2의 실험을 통해 30o 이상의 간격이 자속 변화를 유발하여 최대의 유도기전력을 발생시킴을 확인하였다. 또한, 1열의 자석보다 6열의 자석이 더 큰 유도기전력을 발생시킴을 확인하였다.
이러한 실험 결과로부터 본 연구에서는 Figs. 3(b) 및 3(c)에 나타낸 바와 같이 이온 수송 효과를 증대시키기 위하여 파이프의 길이 방향으로 3열의 자석을 최대한 밀착시킨 15o 간격으로 배치(1 패턴)하였으며, 이러한 패턴을 360o 동안 6번 반복 배치하여 패턴과 패턴 사이의 간격이 30o(15/15/30o)가 되도록 하였다.
RMH Type 3은 Fig. 3(c)와 같이 축 방향으로 각각 7열, 6열, 7열의 자석이 원주 방향 15o 간격으로 배치할 수 있도록 설계되었다. 이 패턴을 원주 방향으로 60o 간격으로 6회 반복하여 RMH Type 3은 원주 방향으로 15/15/30o 간격으로 내/외부 RMH용 자석 각 120개씩 총 240개를 배열하도록 설계되었다. RMH Type 3의 실험에서는 구리 선 대신에 챔버에 수용액을 채우고 구리 전극에 정전압을 인가하여 수전해 실험을 수행하였다.
Fig. 3과 같이 각 RMH 유형의 내부 RMH와 외부 RMH는 동일한 자석 배열을 갖도록 설계되었다. RMH Type 2와 Type 3의 외부 및 내부 RMH는 자석의 인력으로 인해 벨트-폴리 시스템 없이 동일한 속도로 회전할 수 있었다.
2.3 실험 방법
Table 1은 RMH 유형, 자석 강도, 자석 배열, 회전속도, 측정방법에 따라 총 10가지로 구분된다. RMH Type 1 실험은 20o (Case 1), 20/40o (Case 2), 40o (Case 3), 60o (Case 4) 간격으로 자석을 원주 방향으로 배열하여 진행하였다. RMH Type 2는 자석을 원주 방향으로 30o (Case 5) 간격으로 배치한 실험과 15/15/30o (Cases 6과 7) 간격으로 배치한 실험에 사용되었다. RMH Type 3은 자석을 15/15/30o 간격으로 배열하는 실험에 사용되었다(Cases 8-10). Cases 1-6의 실험에서는 지름 10 mm, 길이 10 mm의 네오디뮴 자석을 사용했다. 이 자석들 중 20개 샘플의 자력을 각 2회씩 가우스 미터(TM-801EXP, KANETEC, Japan)로 측정한 결과, 평균 약 4,048 가우스의 자기력을 가지고 있는 것으로 확인되었다.
Cases 7-10에서는 지름 10 mm, 길이 15 mm의 네오디뮴 자석을 사용하였다. 이 자석의 20개 샘플의 자력을 동일한 방법으로 측정한 결과 평균 4,510 가우스의 자기력을 가지고 있는 것으로 확인되었다.
먼저, 수전해 실험 조건을 도출하기 위해 구리 선을 이용하여 회전 자력에 의해 유도되는 전압을 측정하였다. Cases 1-7의 실험에서는 Fig. 4와 같이 수용액 대신에 구리 선을 파이프에 18회 통과시켜 코일을 형성하였다. RMH의 회전 시 발생하는 전압은 전압 측정장치(cDAQ-9178 및 NI 9206, National Instruments Corp., USA)를 이용하여 측정하였다. Fig. 5는 두 챔버 내부에 구리 전극(100 × 100 mm)이 고정된 모습을 보여준다.
Cases 8-10의 실험에서, 챔버에 수용액을 채우고 RMH를 회전시킨 후, 구리 전극에 DC 10 V의 정전압을 인가하여 수전해 실험을 수행하였다. Case 8의 경우 NaCl 15 wt% 수용액, Cases 9, 10은 NaCl 20 wt% 수용액을 사용하였다.
실험은 DC 10 V 정전압의 음극을 자력의 회전에 의해 수소 이온의 수송이 예상되는 전극에 연결하고 양극을 반대극에 연결하여 수행하였다. 먼저 RMH를 회전시키지 않은 상태에서 DC 10 V 정전압을 약 60초간 인가하였다. 그 후, RMH의 회전속도를 약 5초 동안 증가시켜 약 55초(Case 8) 및 약 35초(Case 9) 동안 유지하였으며, 이 과정을 회전속도가 391 RPM이 될 때까지 반복하였다.
Case 10 (NaCl 20 wt%)에서는 RMH의 회전속도를 낮추면서 수전해 실험을 수행하였다. 먼저 RMH를 391 RPM의 속도로 회전시키고 DC 10 V의 정전압을 인가하여 약 30초간 유지하였다. 그 후, RMH의 회전속도를 약 5초 감소시키고 약 25초 동안 유지하였으며, 이 과정을 회전속도가 0이 될 때까지 반복하였다.
3. 결과 및 고찰
본 연구의 목적은 RMH 회전속도, 자석 간격, 자석 수 변화에 따른 회전 자력이 수전해 반응에 미치는 영향을 알아보는 것이다. 이를 위해 구리 배선을 이용한 유도 전압 측정과 NaCl 수용액을 이용한 수전해를 통한 실험적 연구를 수행하였다.
3.1 회전 자력에 의한 전압 신호 측정 결과
수전해의 실험 조건을 알아보기 위해 Cases 1-7의 실험을 통해 회전 자력에 의해 유도된 전압을 측정하여 분석하였다.
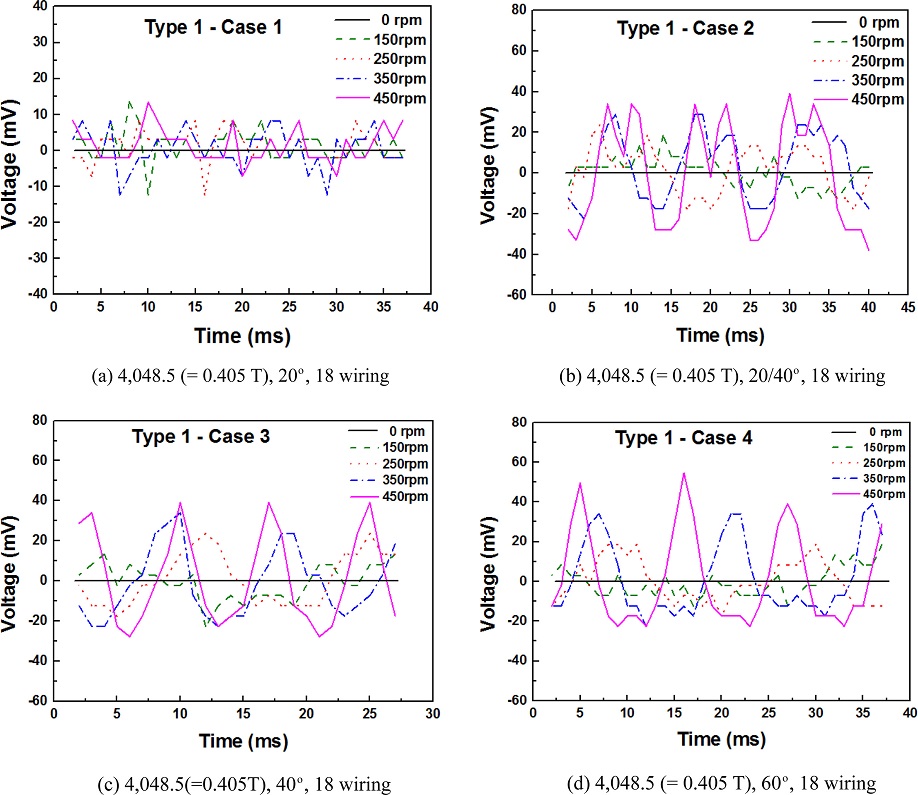
Fig. 6은 RMH Type 1 (Cases 1-4) 의 전압 신호 측정 결과를 나타낸다. Fig. 6(a)는 Case 1의 실험에서 얻은 RMH의 회전속도에 따른 전압 신호를 나타낸 것이다. Case 1은 축 방향으로 1열의 자석을 배치하고, 원주 방향으로 20o 간격으로 18개의 자석(내/외부 RMH 각각)을 배치하였다.
RMH가 회전하지 않을 때는 전압 신호가 측정되지 않았지만, RMH가 회전할 경우 전압 신호가 발생했다. Case 1의 전압 신호의 전위차는 회전속도가 450 RPM일 때 약 15 mV로 측정되었으나 회전속도 증가에 따른 큰 차이는 관찰되지 않았다. 이는 자속을 변화시키기에는 자석 사이의 배열 간격이 너무 짧기 때문인 것으로 생각된다.
Fig. 6(b)는 Case 2의 실험에서 구한 RMH의 회전속도에 따른 전압 신호를 보여주고 있다. Case 2의 실험을 통해 자력의 회전속도가 증가할수록 유도전압이 증가함을 측정하였다. Case 2의 전압 신호의 전위차는 450 RPM에서 약 70 mV로 측정되었다. Case 1과 달리 전압 신호의 마루에서 두 개의 파장을 확인하였으며, 이는 자석의 배치 간격(20/40o)에 따른 현상으로 생각된다.
Fig. 6(c)는 Case 3의 실험에서 얻은 RMH의 회전속도에 따른 전압 신호를 보여준다. 앞의 경우와 마찬가지로 자력의 회전속도가 증가할수록 더 높은 전위차가 유도되는 것으로 측정되었다. 이러한 결과로부터 Case 1에서 사용한 20o는 자석의 배열 간격이 너무 좁아 적합하지 않은 것으로 판단된다. Case 3의 전압 신호의 전위차는 450 RPM에서 약 70 mV로 측정되었으며, Case 2와 같은 마루에서 파장 형태의 전압 신호는 관찰되지 않았다. 이는 자석 배열의 차이 때문이라고 생각된다.
Fig. 6(d)는 Case 4의 실험에서 구한 RMH의 회전속도에 따른 전압 신호를 보여준다. Case 4의 경우 전압 신호의 최대 전위차는 450 RPM에서 약 80 mV에서 측정되었으나, 평균 전위차는 차이는 Cases 2 및 3의 실험 결과와 유사했다.
RMH Type 1을 이용한 Cases 1-4의 실험 결과로부터 자속의 변화를 주기에는 자석 배열 간격 20o가 너무 짧아서 높은 전위차가 발생하지 않는 것으로 판단되었다. 또한, 40o 이상의 모든 자석 배열 간격은 유사한 전위차를 생성할 것으로 생각된다. 또한, RMH 축 방향으로 1열의 자석 배치는 이온 수송을 위한 충분한 동력을 제공하지 못한다고 생각되었다.
Fig. 7는 RMH Type 2 (Cases 5-7)의 전압 신호 측정 결과를 나타낸다. RMH Type 2에서는 자력의 작용 범위를 넓히기 위해 6열의 자석을 축 방향으로 배열하였다.
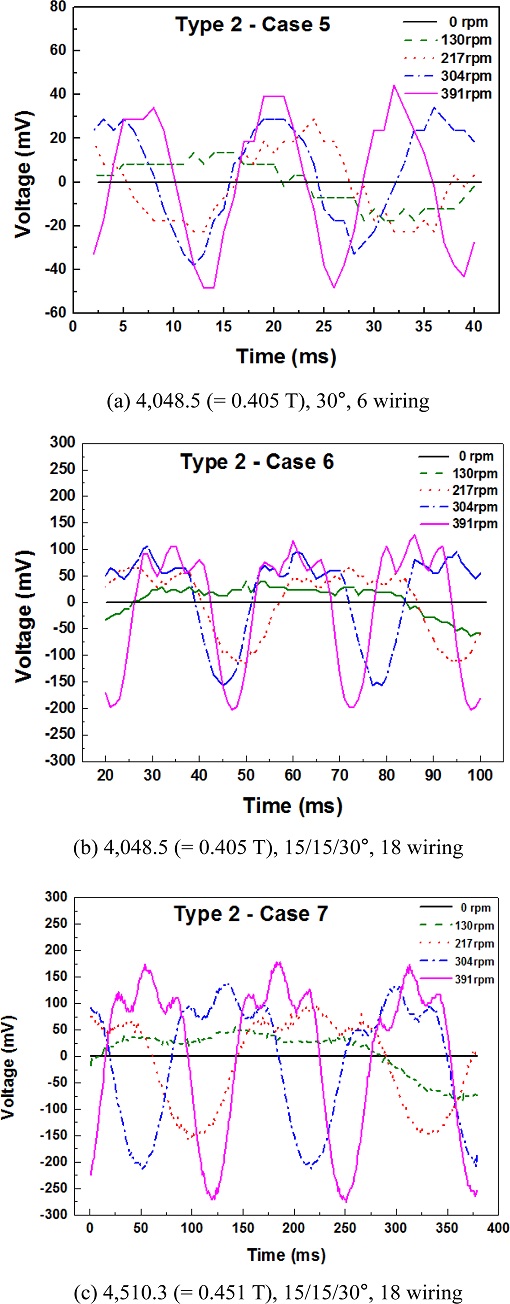
Fig. 7(a)는 Case 5의 실험에서 얻은 RMH의 회전속도에 따른 전압 신호를 나타낸다. Case 5는 원주 방향으로 30o 간격으로 자석을 배치하였다. 전압 신호의 전위차는 391 RPM에서 약 90 mV로 측정되었다. RMH에 장착되는 자석의 수를 늘렸음에도 불구하고 Type 1에 비해 전위차는 크게 증가하지 않았다. 이는 6개의 배선만을 이용하여 측정했기 때문인 것으로 생각된다. 전선의 수가 증가할수록 전위차가 커지므로 18개의 전선으로 동일한 실험을 하면 전선의 수에 비례하여 전위차가 증가할 것으로 예상된다.
Fig. 7(b)는 Case 6의 실험에서 RMH의 회전속도에 따른 전압 신호를 보여주고 있다. Case 6 실험에서는 자석을 원주 방향으로 15/15/30o 간격으로 배치하였다. 전압 신호의 전위차는 391 RPM의 회전속도에서 약 300 mV로 측정되었다.
Case 2의 실험 결과와 같이 전압 신호의 마루에서 3개의 파장이 관찰되었다. 이는 15o 자석 배열 간격에 의한 것으로 생각된다.
Case 5의 결과와 비교하여 Case 6의 배선 수가 18개로 3배 증가함에 따라 전위차는 약 90 mV에서 약 300 mV로 약 3.3배 증가하였다. 또한, 1열의 자석을 축 방향으로 배치한 RMH Type 1 (Cases 2, 3 및 4)과 비교하여 6개의 자석을 축 방향으로 배치했을 때 약 70 mV에서 약 300 mV로 전위차가 약 4.3배 증가하는 것으로 측정되었다.
Fig. 7(c)는 Case 7의 실험에서 RMH의 회전속도에 따른 전압 신호를 보여주고 있다. Case 7에서는 Case 6보다 약 11% 더 강한 자석(4,510 G)을 사용하여 실험을 수행하였다. Case 7에서 측정한 전압 신호의 전위차는 391 RPM의 회전속도에서 약 450 mV였으며, 이는 Case 6보다 약 150 mV 높다. 이 결과로부터 자기력이 약 11% 증가하면 약 50% 증가된 전위차를 생성할 수 있음을 알 수 있다.
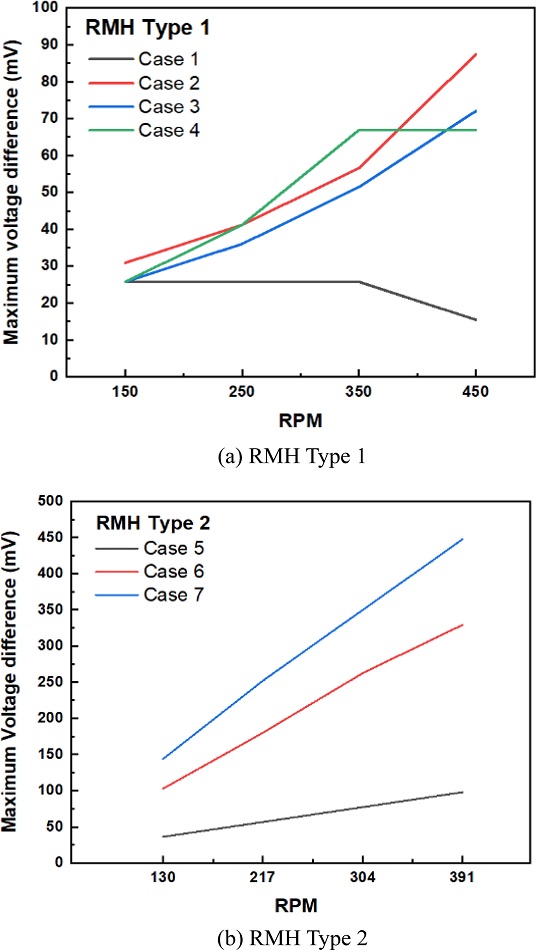
Fig. 8은 실험 결과를 바탕으로, RMH Type 1과 Type 2의 RPM 속도에 따른 최대 전위차를 측정한 결과를 보여주고 있다
Fig. 8(a)는 RMH Type 1 (Cases 1-4)의 RMH 회전속도에 따른 최대 전위차를 측정한 결과를 나타낸다. Cases 2-4의 실험에서는 회전속도가 증가함에 따라 최대 전위차 또한 증가하는 특성을 나타냈다. Case 1의 경우 회전속도의 증가에 따른 큰 차이는 측정되지 않았으며, 450 RPM에서 최대 전위차가 약 15 mV로 감소하였다. 이는 자석 사이의 배열 간격이 20o로 Cases 2-4에 비해 짧기 때문인 것으로 생각된다. Case 2의 경우 최대 전위차가 약 85 mV로 가장 컸으며, Cases 3 및 4와 큰 차이는 없었다. RMH Type 1을 이용한 Cases 1-4의 실험결과로부터 자속의 변화를 주기에는 자석 배열 간격 20o가 너무 짧아서 높은 전위차가 발생하지 않는 것으로 판단되었다. 또한, 40o 이상의 모든 자석 배열 간격은 유사한 전위차를 생성할 것으로 생각된다. 또한, RMH 축 방향으로 1열의 자석 배치는 이온 수송을 위한 충분한 동력을 제공하지 못한다고 생각되었다.
Fig. 8(b)는 RMH Type 2 (Cases 5-7)의 RMH 회전속도에 따른 최대 전위차를 측정한 결과를 나타낸다. Cases 5-7의 경우 회전속도가 증가함에 따라 최대 전위차 또한 증가하는 특성을 나타냈으며, 이는 Cases 1-4의 실험 결과와 유사했다. Case 7의 경우 최대 전위차가 391 RPM에서 450 mV로 Cases 5-7 중 가장 컸으며, Fig. 8(a)의 결과와 비교하여 최대 전위차가 가장 컸던 Case 2보다 약 365 mV 더 증가하였다. 이러한 실험 결과를 바탕으로 최대 전위차가 가장 컸던 Case 7의 경우 수전해 실험 시 가장 좋은 효율을 보여줄 것이라고 생각된다.
RMH Type 1과 Type 2를 이용한 실험 결과는 배관에 전선을 관통시켜서 코일을 형성하고, 전압 측정장치(NI cDAQ-9178, National Instruments, USA)를 이용하여 자기장 회전 시에 발생되는 전압 신호를 측정한 결과를 나타낸다. RMH 회전 시 자력의 세기 및 RMH의 회전속도가 증가함에 따라 전위차가 증가하고 파장이 짧아졌다. 이러한 실험 결과를 바탕으로 자석의 배열, 자력의 세기 및 자기장 회전속도에 비례하여 전하 및 이온의 수송량 및 속도가 증가될 것으로 생각된다.
3.2 알칼리 전기분해에 대한 자기장의 영향
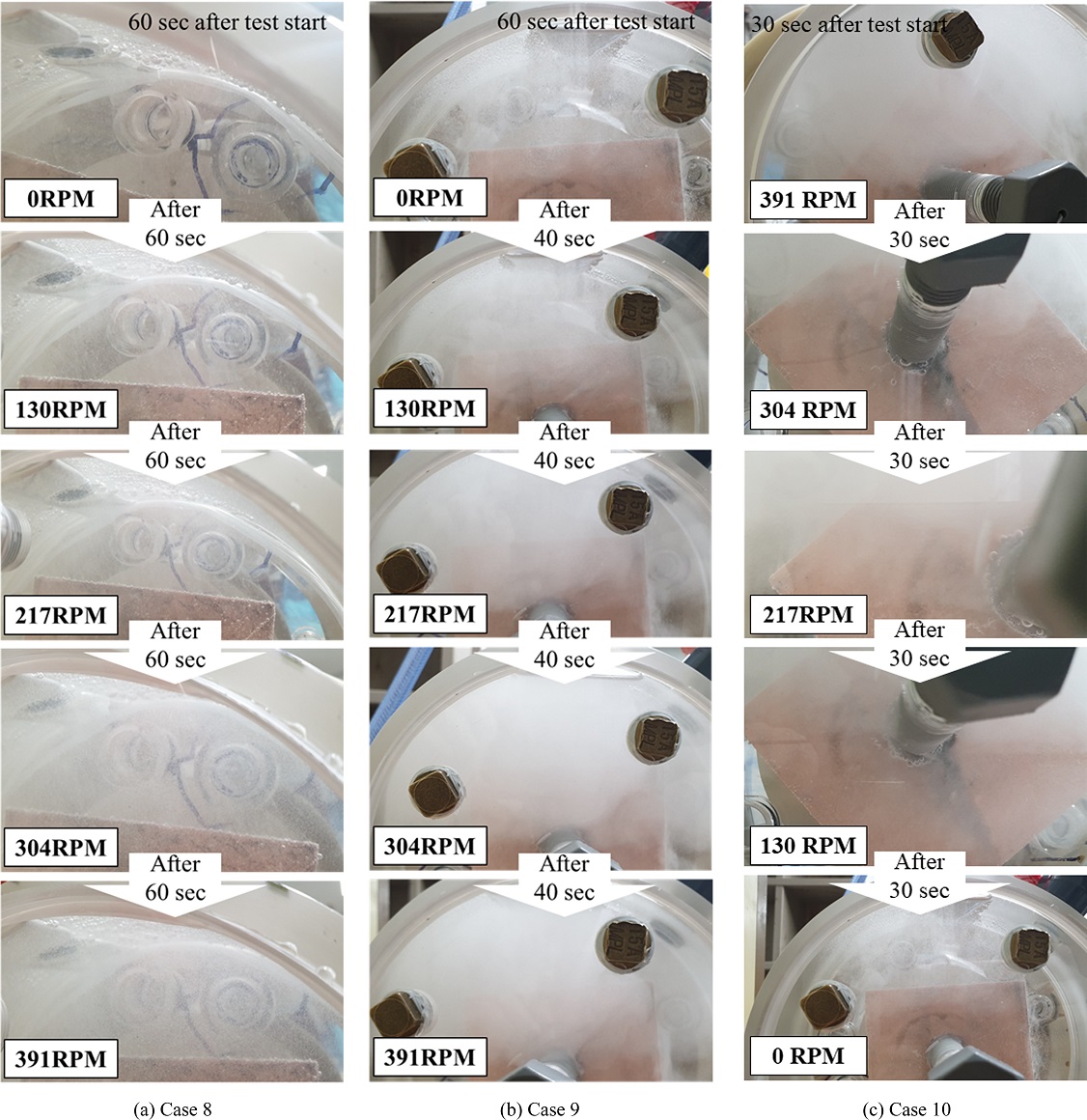
Fig. 9는 RMH의 회전속도, 자석의 간격, 전해질의 농도를 실험 조건으로 선정하고, 수전해 실험에서 자력의 회전에 따른 기포의 양을 관찰한 결과를 나타내며, Cases 8에서 10으로 RMH의 회전속도를 변경하기 직전의 음극의 사진이다. 모든 사진은 같은 날짜에 동일한 조명 아래서 동일한 카메라 셔터스피드(1/60초)로 동일한 실험실에서 촬영되었다.
Fig. 9(a) NaCl 15 wt% 수용액을 이용한 수전해 실험(Case 8)에서 RMH의 회전속도가 증가함에 따라 음극에서 발생하는 기포 사진이다. 전기분해 장치에 정전압을 인가하기 시작한 후 RMH가 회전하지 않고 60초 동안 기다린 후 첫 번째 사진을 촬영했다. 첫 번째 사진 촬영 후 RMH의 회전속도를 약 5초 동안 증가시켰고, 증가된 회전속도를 약 55초 동안 유지한 후 다음 사진을 촬영했다. 동일한 과정을 5회 반복하여 RMH의 회전속도를 최대 391 RPM까지 증가시킨 결과, RMH의 회전속도가 증가할수록 기포의 양이 증가하여 반응 수조 내부가 다수의 작은 기포들이 연기와 유사한 형태로 발생하는 현상을 육안으로 관찰하였으며, 이는 음극에서 발생하는 수소로 생각된다.
Fig. 9(b)는 20 wt% NaCl 수용액을 이용한 수전해 실험(Case 9)에서 RMH의 회전속도가 증가함에 따라 음극에서 발생하는 기포 사진이다. 수전해 실험 장치에 정전압을 인가하기 시작한 후 RMH가 회전하지 않고 60초 동안 기다린 후 첫 번째 사진을 촬영했다.
첫 번째 사진 촬영 후 RMH의 회전속도를 약 5초간 증가시켰고, 증가된 회전속도를 약 35초 동안 유지한 후 다음 사진을 촬영했다. Case 9의 실험 결과에서도 Case 8과 마찬가지로 회전속도가 증가할수록 발생하는 기포의 양이 증가함을 관찰하였다. 또한 Case 8에 비해 유지 시간이 짧음에도 불구하고 반응 수조 내부에 더 많은 기포가 발생하여 반응 수조 내부를 육안으로 확인하기 어려울 정도로 뿌옇게 되는 현상을 관찰하였다. Case 9의 결과를 통해 수용액의 농도와 수전해 반응속도는 밀접한 관련이 있다고 생각된다.
Moon and Pak [9]과 Gilliam 등[10]은 수용액 농도가 수소 생성에 비례하는 경향이 있으며, 약 30% KOH 조건에서 가장 높은 수소 생성을 보였다고 보고하였다. Iida et al. [15]은 정전류를 이용한 수전해 실험에서 수용액의 농도에 따라 IR-Drop의 감소를 보고하였다. 본 연구에서는 정전압을 사용하였기 때문에 수용액의 농도가 증가할수록 반응속도가 증가한다고 생각할 수 있다. 이는 수용액에 더 많은 이온이 존재하고 자력에 의해 수송되는 이온의 수가 증가하기 때문이라고 생각된다.
Cases 8과 9의 실험 결과는 RMH의 회전속도에 관계없이 실험시간이 증가할수록 수전해 반응속도가 증가함을 알 수 있다. 따라서 실험시간이 물의 전기분해에 미치는 영향을 관찰하기 위하여 Case 9와 동일한 조건에서 RMH의 회전속도를 감소시키면서 실험(Case 10)을 수행하였다.
Fig. 9(c)는 NaCl 20 wt% 수용액을 이용한 수전해 실험(Case 10)에서 RMH의 회전속도가 감소함에 따라 음극에서 발생하는 기포 사진이다. 수전해 실험 장치에 정전압과 RMH 회전을 인가하기 시작한 후 30초를 기다린 후 첫 번째 사진을 촬영했다. 첫 번째 사진 촬영 후 RMH의 회전속도를 약 5초간 감소시키고 약 25초 동안 감소된 회전속도를 유지한 후 다음 사진을 촬영했다. 동일한 과정을 5회 반복하여 RMH의 회전속도를 391 RPM에서 0 RPM까지 감소시켰다.
실험 시작 시 RMH는 391 RPM의 속도로 회전하고 동시에 정전압을 인가하였다. 그 결과 Fig. 9(c)와 같이 수전해 반응에 의한 기포가 매우 활발하게 발생하였다. 또한, RMH의 회전속도가 감소할수록 기포 발생량이 감소함을 관찰하였다. Cases 9, 10의 결과로부터 자기력의 회전속도와 수전해 반응속도는 매우 밀접한 관련이 있는 것으로 생각된다.
Fig. 9에 도시된 음극과 달리, 양극에서는 명백한 기포 발생이 관찰되지 않았다. 대신, 양극 부근의 수용액에서 청색 물질이 생성됨을 관찰하였다. NaCl 수용액과 구리 전극을 사용하였기 때문에 양극에서 염소 이온이 구리와 반응하여 염화구리 화합물이 생성된 것으로 생각된다.
본 연구를 통해 회전 자력과 수전해 반응속도 사이에 관계가 있음을 관찰하였다. 그 결과 회전하는 자력을 이용하여 전기를 발생시키는 것과 같은 방식으로 이온을 수송하는 것이 가능하다고 생각되며, 이 현상을 이용하여 수전해 반응의 속도를 향상시키는 것도 가능하다고 생각된다.
4. 결론
총 3종의 RMH를 설계 및 제작하였다. 또한 회전 자력을 이용한 수전해 반응의 효율을 향상시키기 위한 실험적 연구를 수행하였다. 본 연구를 통해 얻은 결론은 다음과 같다.
(1) RMH Type 1과 Type 2를 사용하고 배선을 이용하여 전압을 측정한 Cases 1-5의 실험 결과로부터 자속 변화를 일으키기에는 20o의 자석 배열 간격이 너무 짧은 것으로 판단되었다. 또한, 40o 이상의 모든 자석 배열 간격은 유사한 전위차를 생성할 것으로 판단된다. 측정된 전압 신호의 전위차와 자석의 배열을 고려하면 본 연구에서는 30o의 자석 배열 간격이 가장 이상적이라고 생각된다.
(2) RMH의 축 방향 자석의 개수를 1개에서 6개로 늘린 결과, 자력이 작용하는 구간이 확대되었고, 생성된 전압 신호는 70-약 300 mV로 전위차가 약 4.3배 증가하였다.
(3) 사용하는 자석의 자력을 약 4,049 G에서 약 4,510 G로 약 11% 증가시킨 결과, 생성된 전압 신호의 전위차가 약 300 mV에서 약 450 mV로 약 50% 증가하는 것으로 측정되었다.
(4) 배선을 이용한 실험 결과로부터 자기장의 배열, 회전속도 및 세기를 변화시킴으로써 이온수송을 조절할 수 있다고 생각된다.
(5) RMH Type 3을 이용한 Cases 8~10의 실험에서 RMH의 회전속도가 증가할수록 수전해 반응에 의해 발생하는 기포의 양이 증가함을 관찰하였다. 이는 회전하는 자력에 의한 이온수송에 의한 현상으로 생각되며, 이 현상을 이용하여 수전해 반응의 효율을 향상시킬 수 있다고 생각된다.
NOMENCLATURE
| PEM : | Polymer Electrolyte Membrane |
| HTE : | High Temperature Electrolysis |
| AE : | Alkaline Electrolysis |
| RMH : | Rotary Magnet Holder |
| RPM : | Revolutions per Minute |
Acknowledgments
본 연구는 군산시가 지원하는 지역맞춤형 전기차 클러스터 전문인력 양성사업과 교육부의 재원으로 한국연구재단(NRF)의 지원을 받아 수행된 과학기술분야 기초연구사업(NRF-2019R1I1A3A01062764)에 의해 지원되었음.
REFERENCES
-
Chauveau, F., Mougin, J., Mauvy, F., Bassat, J.-M., Grenier, J.-C., (2011), Development and operation of alternative oxygen electrode materials for hydrogen production by high temperature steam electrolysis, International Journal of Hydrogen Energy, 36(13), 7785-7790.
[https://doi.org/10.1016/j.ijhydene.2011.01.048]

-
Nagai, N., Takeuchi, M., Kimura, T., Oka, T., (2003), Existence of optimum space between electrodes on hydrogen production by water electrolysis, International Journal of Hydrogen Energy, 28(1), 35-41.
[https://doi.org/10.1016/S0360-3199(02)00027-7]

-
Kaninski, M. P. M., Stojić, D. L., Šaponjić, Đ. P., Potkonjak, N. I., Miljanić, Š. S., (2006), Comparison of different electrode materials-nergy requirements in the electrolytic hydrogen evolution process, Journal of Power Sources, 157(2), 758-764.
[https://doi.org/10.1016/j.jpowsour.2005.10.105]

-
De Souza, R. F., Padilha, J. C., Gonçalves, R. S., De Souza, M. O., Rault-Berthelot, J., (2007), Electrochemical hydrogen production from water electrolysis using ionic liquid as electrolytes: Towards the best device, Journal of Power Sources, 164(2), 792-798.
[https://doi.org/10.1016/j.jpowsour.2006.11.049]

-
De Souza, R. F., Padilha, J. C., Gonçalves, R. S., Rault-Berthelot, J., (2006), Dialkylimidazolium ionic liquids as electrolytes for hydrogen production from water electrolysis, Electrochemistry Communications, 8(2), 211-216.
[https://doi.org/10.1016/j.elecom.2005.10.036]

-
Nikolic, V. M., Tasic, G. S., Maksic, A. D., Saponjic, D. P., Miulovic, S. M., Kaninski, M. P. M., (2010), Raising efficiency of hydrogen generation from alkaline water electrolysis-Energy saving, International Journal of Hydrogen Energy, 35(22), 12369-12373.
[https://doi.org/10.1016/j.ijhydene.2010.08.069]

-
Licht, S., Wang, B., Mukerji, S., Soga, T., Umeno, M., Tributsch, H., (2001), Over 18% solar energy conversion to generation of hydrogen fuel; Theory and experiment for efficient solar water splitting, International Journal of Hydrogen Energy, 26(7), 653-659.
[https://doi.org/10.1016/S0360-3199(00)00133-6]

-
Zhang, H., Lin, G., Chen, J., (2010), Evaluation and calculation on the efficiency of a water electrolysis system for hydrogen production, International Journal of Hydrogen Energy, 35(20), 10851-10858.
[https://doi.org/10.1016/j.ijhydene.2010.07.088]

-
Moon, K., Pak, D., (2015), The characteristics of hydrogen production according to electrode materials in alkaline water electrolysis, Journal of Energy Engineering, 24(2), 34-39.
[https://doi.org/10.5855/ENERGY.2015.24.2.034]

-
Gilliam, R., Graydon, J., Kirk, D., Thorpe, S., (2007), A review of specific conductivities of potassium hydroxide solutions for various concentrations and temperatures, International Journal of Hydrogen Energy, 32(3), 359-364.
[https://doi.org/10.1016/j.ijhydene.2006.10.062]

-
Kim, J., Jun, A., Gwon, O., Yoo, S., Liu, M., Shin, J., Lim, T.-H., Kim, G., (2018), Hybrid-solid oxide electrolysis cell: A new strategy for efficient hydrogen production, Nano Energy, 44, 121-126.
[https://doi.org/10.1016/j.nanoen.2017.11.074]

-
Matsushima, H., Bund, A., Plieth, W., Kikuchi, S., Fukunaka, Y., (2007), Copper electrodeposition in a magnetic field, Electrochimica Acta, 53(1), 161-166.
[https://doi.org/10.1016/j.electacta.2007.01.043]

-
Bund, A., Koehler, S., Kuehnlein, H., Plieth, W., (2003), Magnetic field effects in electrochemical reactions, Electrochimica Acta, 49(1), 147-152.
[https://doi.org/10.1016/j.electacta.2003.04.009]

- Yun, U. H., Jung, J. S., Kim, J. G., (2017), A study on ionic wind distribution characteristics according to magnetic field in needle-to-ring electrode, Proceedings of the Korean Institute of Illuminating and Electrical Installation Engineers Annual Conference, 77. http://www.dbpia.co.kr/Article/NODE07268405
-
Iida, T., Matsushima, H., Fukunaka, Y., (2007), Water electrolysis under a magnetic field, Journal of the Electrochemical Society, 154(8), E112.
[https://doi.org/10.1149/1.2742807]

-
Matsushima, H., Kiuchi, D., Fukunaka, Y., (2009), Measurement of dissolved hydrogen supersaturation during water electrolysis in a magnetic field, Electrochimica Acta, 54(24), 5858-5862.
[https://doi.org/10.1016/j.electacta.2009.05.044]


B.Sc. candidate in the Department of Mechanical Engineering, Kunsan National University. His research interest is mechanic and hydrogen energy.
E-mail: khj0069@kunsan.ac.kr

B.Sc. candidate in the Department of Mechanical Engineering, Kunsan National University. His research interest is mechanics.
E-mail: gwanyongjeong@kunsan.ac.kr

Ms. in the Department of Mechanical Engineering, Kunsan National University. His research interest is mechanics.
E-mail: guohao8963@gmail.com

Professor in the Department of Mechanical Engineering, Kunsan National University. His research interest is in the material, fatigue and fracture, mechanic and hydrogen energy.
E-mail: sangyoungkim@kunsan.ac.kr