형상기억 고분자의 회전형 적층제조를 통한 이중 변형 혈관 스텐트 제작
Copyright © The Korean Society for Precision Engineering
This is an Open-Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
In this study, we present the fabrication of dual-morphing vascular stents using an additive-lathe printing method and two different shape-memory polymers. Traditional additive manufacturing techniques confront significant challenges in producing vascular stents with complex, hollow, mesh-like structures due to limitations such as a flat printing bed and the placement of supports. To overcome these obstacles, we employed a lathe-type additive manufacturing system with a rotatable base substrate, enabling precise fabrication of cylindrical-shaped stents. To achieve shape transformability, we used shape-memory polymers as the stent materials, offering the advantage of minimally invasive surgery. Two distinct shape-memory polymers, with different transition temperatures (35 and 55oC), were printed using the additive-lathe method. The printed stents consisted of two distinct parts that underwent dual-stage morphological changes at the different temperatures. By manipulating the printing paths, the dual-morphing properties of the stents could be adjusted in both longitudinal and circumferential directions. This innovative approach could be a solution to several limitations associated with the application of stents in diseased vascular tissues with complex shapes, facilitating minimal invasion during surgical procedures.
Keywords:
Additive manufacturing, Shape memory polymer, Vascular stent, 4D printing키워드:
적층 제조, 형상기억 폴리머, 혈관 스텐트, 4D 프린팅1. 서론
적층제조 공정은 1990년대에 들어 금형없이 다양한 3차원 형상을 빠르고 효율적으로 제조할 수 있는 이점을 살려 시제품 제작을 위한 쾌속조형기술로서 널리 활용되어 왔다[1]. 최근에는 폴리머, 세라믹, 금속 및 복합재료와 같은 다양한 소재를 사용하여 자동차, 항공우주, 의료분야 등에 직접적으로 활용될 수 있는 제품을 제작할 수 있는 수준으로 발전되어 왔다. 적층제조 공정 중 하나인 재료압출(Material Extrusion, MEX) 공정은 폴리머 기반 적층제조 공정의 대표적 방식으로서 폭넓은 재료 선택의 장점이 있다[1,2]. 재료의 선택이 자유롭기 때문에 생체적합성, 전기전도성, 연/경질 기계적 물성 등을 갖는 기능성 재료를 활용한 많은 연구가 이루어지고 있다[3-6].
이러한 기능성 재료로서 최근 형상기억 폴리머(Shape Memory Polymer, SMP)에 대한 관심이 높아지고 있다. SMP는 특정 온도 및 습도와 같은 환경 변화에 의해 물리적으로 변형된 형상이 원래의 형상으로 복원되는 기능을 가진 폴리머로, 의료, 우주, 소프트 로봇분야 등 다양한 응용 분야에서 연구가 이루어지고 있다. 이러한 SMP 소재를 적층제조 공정에 활용함으로써 환경 요인 변화 및 시간 경과에 따라 변형하는 구조를 제작하는 ‘4D 프린팅’ 기술이 관심을 받고있다[7-9].
의료분야의 혈관 스텐트 제작에 있어 4D 프린팅 기술을 활용한 많은 연구가 진행되고 있다[10,11]. 혈관 스텐트는 혈관 내부에 삽입되어 혈관을 확장시키는 의료기기로, 혈관 폐색이나 협착을 치료하기 위해 사용된다[12]. 일반적으로 사용되는 금속 스텐트는 물리적인 힘으로 형상변화를 일으켜 혈관을 확장하지만, SMP로 제작된 스텐트는 삽입 이후 자가적으로 형상변화를 일으키기 때문에 보조 장비의 사용 및 침습 수술 부위를 최소화 할 수 있는 장점이 있다[13]. 따라서 SMP를 사용한 혈관 스텐트는 기존의 금속 스텐트와 비교해 더 나은 회복 속도 및 치료 효과를 기대할 수 있다[14]. 현재까지는 대부분 단일 재료의 SMP로 제작한 혈관 스텐트가 주로 연구되어 왔다[10]. 하나의 SMP 소재만을 사용할 경우, 형상복원이 단조롭게 한가지 형태로만 일어나게 된다. 이는 복잡한 혈관 네트워크 내에서 스텐트의 침습이 단계적으로 이뤄져야 할 경우 시술의 공간적 제약이 따를 수 있다[15].
본 연구에서는 두 가지 서로 다른 SMP 소재를 복합 프린팅하여 스텐트를 제작하고, 제작된 스텐트의 두 단계에 걸친 형상변화 특성을 검증함으로써 기존 단일재료 SMP 스텐트의 한계점 극복 가능성을 확인하고자 한다. 두 종류의 SMP는 각각 35oC와 55oC에서 반응하여 변형회복이 일어난다. 따라서 제작된 스텐트는 온도변화에 따라 각 온도에서 두 단계의 형상변화를 하게 된다. 일반적으로 혈관 스텐트의 경우 적절한 변형성 및 강성을 갖기 위해 메쉬(Mesh) 패턴을 가진 중공 원통(Hollow Cylinder)의 형태로 제작된다. 기존 상향 적층 3D 프린팅 방식으로 이러한 형태를 제작할 경우, 용융 폴리머의 불안정한 유변학적 특성과 지지대(Support) 배치의 어려움으로 인해 제조 형상의 정밀도가 떨어지게 된다. 따라서 본 연구에서는 회전형 적층제조 시스템을 통해 SMP 소재를 프린팅하여 메쉬형 혈관 스텐트를 제작한다. 회전형 3D 프린팅 공정 방식을 채택함으로써 복잡한 메쉬 패턴 형상의 혈관 스텐트를 효율적으로 제작할 수 있었으며, 이를 통해 혈관 스텐트의 형상 정밀도 향상 및 이중 변형성을 확보할 수 있었다.
2. 재료 및 방법
2.1 회전형 3D 프린터
기본 프린팅 시스템은 필라멘트 형태의 열가소성 폴리머를 용융하여 노즐을 통해 분사하는 FFF (Fused Filament Fabrication)방식으로 구성하였다. 회전형 3D 프린터(Lathe-type 3D Printer)는 제작 플랫폼(Build Platform)을 보편적인 카테시안 좌표계(Cartesian Coordinate System) 기반의 평판 프린팅 베드(Flat Printing Bed)에서 원통 형태의 맨드릴(Mandrel)로 대체한 것이다[16]. 회전형 3D 프린터의 펌웨어(Firmware)는 오픈소스인 Marlin을 사용하였으며 G-code는 오픈소스 슬라이싱 소프트웨어인 Cura를 사용했다. 본 연구에서 사용된 맨드릴은 직경 8 mm, 길이 200 mm이다. PVA (Poly-vinylalcohol) 필라멘트 (PVA 필라멘트, 1.75 mm, eSUN Ltd., 중국)를 스텐트가 제작될 영역에 사전에 프린트하여 안정적인 적층이 이루어지도록 하였다. PVA 프린팅에 사용된 노즐의 직경은 0.4 mm, 압출온도 210oC, 압출 속도는 15 mm/s 이다.
2.2 형상기억 폴리머(SMP)
35oC와 55oC의 두 가지 서로 다른 유리전이온도(Tg)를 갖는 열가소성 폴리우레탄(Thermoplastic Polyurethan, TPU) 기반의 SMP 원재료를 사용하였다(NGM3520, NGM5520, Ether Type, Nanografi, Turkey). NGM3520과 NGM5520은 각각 35oC와 55oC 이상에서 이전 변형상태로 형상복원이 일어나는 특징을 갖는다. 원재료는 펠렛(Pellet) 형태로 주어지며 이를 압출기(필리봇 H400, 포던테크, 한국)를 사용하여 필라멘트 형태로 가공하였다. NGM3520와 NGM5520 재료는 각각 180oC와 210oC에서 압출 하였으며 필라멘트 압출기의 노즐 직경은 1.2 mm, 압출 속도 10 mm/s이다. 최종적으로 프린팅용으로 제작한 NGM3520 및 NGM5520 필라멘트는 직경 1.75 mm에 맞추어 압출하였다.
3. 결과 및 고찰
3.1 SMP의 프린팅 특성
회전형 적층제조 기반 SMP 스텐트를 제작하기에 앞서, SMP의 최적 프린팅 공정변수를 찾는 사전 테스트를 수행하였다. 일반적으로 권장되는 TPU의 프린팅 속도인 10 mm/s와 온도 210oC 조건을 초기설정으로 두고 스텐트 메쉬 패턴을 2차원 평면으로 제작한 결과, 패턴 형상이 불명확하며 재료의 압출이 과하게 이루어졌다(Fig. 1(a)). 프린팅 속도를 20 mm/s로 제작한 결과 적절한 메쉬 패턴이 제작되었으며 과도한 압출 또는 미형성된 패턴 부위가 관찰되지 않았다(Fig. 1(b)). 40 mm/s의 속도로 제작한 경우, 과도한 프린팅 속도로 인해 노즐에서 새어 나온 용융된 폴리머가 패턴 내부에서 실처럼 늘어지는 결함(Stringing)과 패턴의 두께가 얇아지는 현상이 발견되었다(Fig. 1(c)). 이와 같이 메쉬 패턴이 적절한 형태로 형성되는 조건을 NGM3520 그리고 NGM5520 두 가지 재료에 대해 실험적 시행 착오를 통해 찾았다. 그 결과 두 재료 공통적으로 20 mm/s의 프린팅 속도로 제작하였으며, NGM3520은 210oC, NGM5520은 235oC의 노즐 온도로 각각 설정하였다.
3.2 회전형 3D 프린터
전술한 바와 같이 일반적인 평판형 베드 프린팅 방식과 비교해 회전형 3D 프린팅 방식은 중공형태의 구조물을 제작하는데 장점이 있다[16]. 특히, 복잡한 메쉬패턴을 갖는 원통형 혈관 스텐트와 같은 구조물을 제작하는 데에 특화시킬 수 있다(Fig. 2(a-i)). 스텐트는 회전형 3D 프린팅을 통해 20 mm/s의 속도로 제작되었으며, 결함 없이 제작된 것을 확인할 수 있다. 이는 용융된 폴리머가 불안정한 유변학적 특성을 갖더라도 맨드릴 표면에 적층하기 때문에 지지대가 필요하지 않기 때문이며, 용융된 폴리머가 실처럼 늘어지는 결함과 형상이 무너지는 결함(Collapsing)이 발생하지 않았다. Fig. 2(a-ii)에서 보는 바와 같이 평판 프린팅 베드를 사용하는 전통 방식의 3D 프린터에서 같은 형상을 제작할 경우 매우 불안정한 형태로 적층된다. 또한 제작 된 메쉬패턴에서 수많은 Stringing 결함이 발생함을 확인하였다.
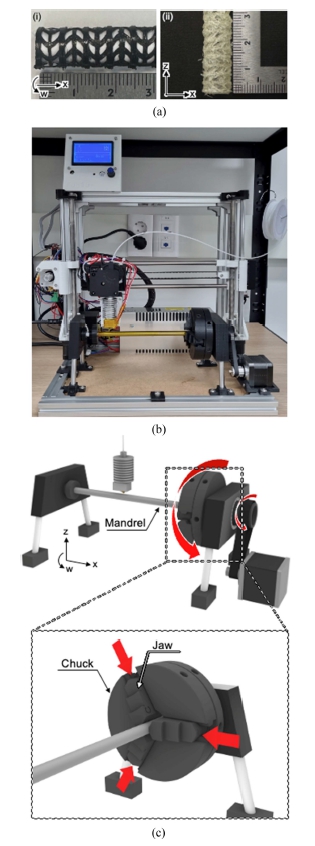
(a) Mesh-form stents printed by (i) additive-lathe 3D printing system and (ii) conventional 3D printer with flat bed. (b) Lab-made additive-lathe machine. (c) Schematic illustration of working parts in the additive-lathe machine
또한 스텐트 형상을 이종 재료의 복합된 형태로 제작하는 경우, 회전형 3D 프린팅 방식이 더욱 장점을 보인다. 기존 평판형 프린팅 방식은 공정 중 적층방향(z축)에서 다른 재료의 사용을 위해 재료 변경 과정이 필요하며 이를 위해 이중 노즐(Dual Nozzle) 방식의 3D 프린터를 사용한다[17]. 이러한 경우 같은 적층면이 바뀔 때마다 잦은 노즐 교체로 인해 제작물의 품질이 저하될 수 있다. 반면, 회전형 3D 프린터에서는 맨드릴의 둘레 방향 및 길이방향으로 같은 반경면에서 적층이 이루어지기 때문에 재료 변경 과정을 상대적으로 줄일 수 있는 이점이 있다.
Fig. 2(b)는 제작한 회전형 3D 프린터이다. 알루미늄 프로파일을 기본 틀로 사용하였고 부수적인 부품들은 PLA 필라멘트(Moment 사, 한국)를 통해 별도로 3D 프린팅하여 제작하였다. 기존의 회전형 3D 프린터의 경우, 베어링이나 커플러로 맨드릴을 고정하여 사용하기 때문에 다양한 지름의 맨드릴을 사용할 수 없는 단점이 있다. 이 문제를 해결하기 위해 Fig. 2(c)와 같이 맨드릴 고정 부위를 선반의 척(Chuck) 형태로 제작하여 다른 지름을 같는 맨드릴을 자유롭게 교체하여 사용할 수 있도록 했다. 맨드릴은 고정부 척의 죠우(Jaw)를 통해 고정되며 회전부와 함께 회전하며 표면에 프린팅이 이루어질 수 있도록 제작하였다. 그리고 오픈소스로 제공되는 선반 척 모델에서 기어 부분을 추가하여 모터와 연결된 타이밍 벨트에 의해 회전할 수 있도록 설계하였으며 3D 프린팅을 통해 척과 기어를 제작하였다.
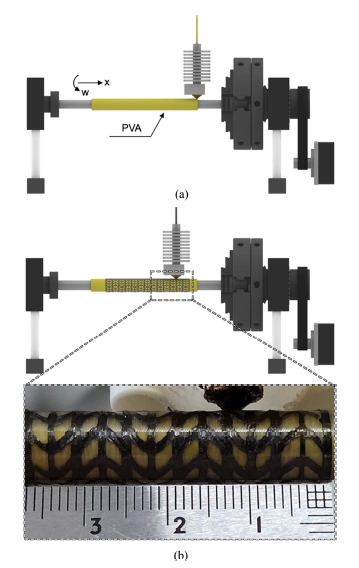
3.3 PVA 코팅 맨드릴을 사용한 스텐트 제작
회전형 3D프린터를 통하여 제작된 적층 구조물은 맨드릴의 표면과 구조물의 내측면이 전체적으로 부착되어 있으며, 이러한 부착력은 안정적인 회전 적층을 위해 필수적이다. 반면 적층이 완료된 후에는 이 부착력으로 인해 구조물과 맨드릴을 분리하기 매우 어려우며, 분리과정 중에 적층 구조물의 손상이 일어날 수 있다.
따라서 제작한 중공 형태의 혈관 스텐트와 맨드릴을 분리하는 과정 중 발생가능한 스텐트의 손상을 최소화하기 위해, 프린팅 맨드릴에 수용성 재료인 PVA 재료를 한 층 프린팅함으로써 표면 코팅을 하였다(Fig. 3(a)). 이후 PVA 코팅 맨드릴 표면에 스텐트 구조물을 적층제조하여 완성하고, PVA 코팅층을 물에 녹여 제거함으로써 제조된 혈관 스텐트와 맨드릴 사이에 공간적 여유를 발생시킬 수 있다. 이러한 공간적 여유에 의해 제조된 스텐트를 쉽게 분리할 수 있으며, 강제적인 물리적 힘이 가해지지 않기 때문에 스텐트 구조물의 손상이 최소화될 수 있다.
3.4 이중 변형 혈관 스텐트 설계 및 제작
변형회복 온도가 서로 다른 두 종류의 SMP를 이용하여 혈관 스텐트의 형상 변화가 두 단계에 걸쳐 일어날 수 있도록 메쉬 패턴을 제작하였다(Figs. 3(b) 및 4(a)). 메쉬 패턴의 설계는 상용 스텐트에서 많이 사용하는 벌집(Honey Comb) 및 오그제틱(Auxetic) 구조 디자인을 참조하였다[18,19].
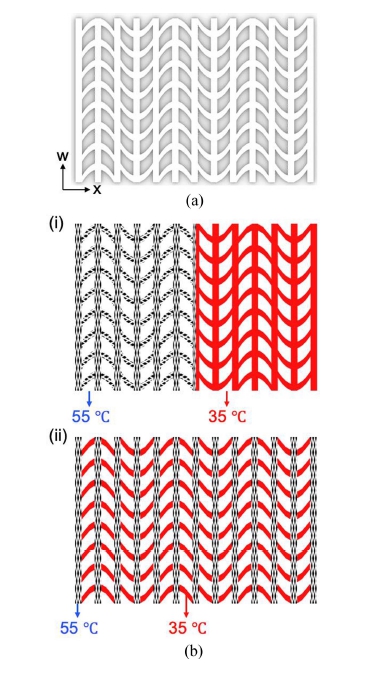
(a) Mesh pattern of stent. (b) Dual composition of two different SMP materials for dual-morphing transformation in (i) longitudinal and (ii) longitudinal/circumferential ways
원주방향의 뼈대와 이를 각각 연결하는 물결 무늬의 메쉬를 폭 0.1 mm 및 두께 0.4 mm로 프린팅 제작하였다. 각 뼈대와 메쉬 부분에 다른 재료를 배치함으로써 변형 형태가 다른 두 가지 설계를 제안하였다. 첫 번째로 55oC와 35oC에 형상회복이 일어나는 SMP (NGM5520와 NGM3520)를 길이방향으로 이어 배치하여 길이방향의 이중 형상복원이 일어날 수 있게끔 설계하였다. 이 설계안은 사용자의 판단에 따라 길이방향으로 팽창되는 길이 조절이 가능하다. Fig. 4(b-i)의 파란색 영역은 NGM5520을 사용하였으며 빨간색 영역은 NGM3520을 사용하였다. 회전형 적층제조 공정을 통해 NGM5520의 파란색 영역 제작완료 이후, 재료를 NGM3520으로 변경하여 빨간색 영역을 제작하였다. 또한 서로 다른 재료가 맞닿는 부위를 뼈대 폭의 절반(0.5 mm)만큼 중첩 프린팅함으로써 각 부위를 연결하였다. 길이방향으로 배치된 서로 다른 SMP에 의해 온도가 상승함에 따라 형상복원 온도가 낮은 재료인 NGM3520부터 변형이 시작되며, 이후 추가 온도 상승에 의해 NGM5520 부위의 변형이 이루어진다.
두 번째 설계안으로는 스텐트가 길이방향과 원주방향으로 형상의 단계적 복원이 가능하도록 디자인하였다(Fig. 4(b-ii)). 이는 압축된 스텐트를 길이 방향으로 먼저 확장시켜 병변으로 좁아진 혈관에 적절하게 위치시킨 후, 원주방향으로 팽창하여 병변 혈관 부위를 확장시키는 기능을 가진다. NGM3520을 사용해 뼈대(파란색)를 제외한 빨간색 영역을 제작한 뒤, NGM5520를 사용해 파란색 영역의 뼈대를 제작함으로써, 35oC에서의 길이 방향 확장 및 55oC에서의 원주방향으로 팽창이 순차적으로 일어난다.
3.5 이중 변형 혈관 스텐트의 형상복원 과정
혈관 스텐트는 일시적으로 형상이 압축된 상태로 환자의 몸에 삽입되며, 표적 위치에서 팽창하여 심혈관계 질환으로 좁혀진 혈관의 개존율(Patency Rate)을 회복한다[12]. 따라서 혈관 스텐트는 수축된 상태와 팽창된 상태로 그 형태와 구분되고, 표적 위치에 도달하기 전까지는 수축시킨 형태를 유지하게 된다. SMP기반의 스텐트는 먼저 팽창된 형상을 기준으로 제작하고 이를 압축상태로 고정한다. SMP는 유리전이온도 이상에서 물리적인 힘으로 압축이 가능하며, 압축을 유지시킨 상태에서 온도를 유리전이온도 이하로 떨어뜨릴 경우 압축력을 제거하여도 변형상태의 형상이 고정된다[20,21]. 제작된 스텐트를 두 SMP의 유리전이온도 이상의 온도인 60oC의 온수에 담가 물리적인 힘을 가해 길이 및 원주 방향으로 압축시켰다. 압축을 유지한 상태로 얼음물에 담가 온도를 0oC 이하로 떨어뜨려 형태를 일시적으로 고정시켰다(Figs. 5(a-i) 및 5(b-i)).

Shape recovery of dual-morphing vascular stents in (a) longitudinal and (b) longitudinal/circumferential directions
첫 번째 설계안으로 제작된 스텐트는 Fig. 5(a)에서 볼 수 있듯이 길이방향으로 두 단계에 걸쳐 형상이 복원되었다. 압축 고정된 스텐트를 35oC 이상 55oC 이하의 온수에 담가 NGM3520으로 제작된 부분의 1차 형상복원을 유도하였다(Fig. 5(a-ii)). 다음으로 NGM5520으로 제작된 부분의 2차 형상복원을 위해 스텐트를 55oC 이상의 따듯한 물에 담가 수축 전 원래의 형태로 복원이 됨을 확인하였다(Fig. 5(a-iii)). 이 스텐트는 길이방향으로의 형상 변형이 가능하도록 설계된 것으로, 스텐트 시술 환경에서 주어진 병변 부위의 범위에 맞추어 길이를 조절할 수 있다.
두 번째 설계안은 동맥경화(Arteriosclerosis)와 같은 질환의 시술에 특화된 형상으로서 병변으로 좁혀진 공간을 통과하고 팽창시킴으로써 해당 부위를 확대하는 기능을 갖는다(Fig. 5(b)). 길이방향과 원주방향으로 압축 고정된 스텐트는 35oC 이상 55oC 이하의 온도에서 NGM3520으로 제작된 부분이 길이방향으로 1차 형상복원 되어 좁은 병변 부위를 통과할 수 있다(Fig. 5(b-ii)). 둘레의 뼈대에 사용된 NGM5520은 55oC 이상의 온도에서 반응하며, 원주방향으로 2차 형상복원되어 좁은 병변부위를 확대하는 기능을 한다(Fig. 5(b-iii)).
4. 결론
본 연구에서는 회전형 3D 프린팅 시스템을 제작하고 이를 활용하여 SMP 기반의 혈관 스텐트를 제작하였다. 스텐트는 메쉬 패턴을 갖는 중공 형태의 구조물로서, 일반적인 카테시안 좌표계 평판 적층제조 방식에서는 용융 폴리머의 불안정한 유변학적 특성 및 지지대 배치의 어려움으로 인해 제작 안정성이 매우 떨어진다. 따라서 본 연구에서는 회전형 3D 프린팅 방식을 채택하였으며, 이를 통해 일반적인 평판방식 3D 프린팅 공정에 비해 안정적으로 메쉬 패턴 중공 구조물을 제작할 수 있음을 확인하였다. 회전 프린팅을 위한 맨드릴 표면에 PVA 층을 프린팅하여 형성함으로써 스텐트 구조물 제작 이후 맨드릴 과의 분리를 용이하게 하였다. 또한 형상복원 온도가 다른 두 종류의 SMP를 복합적으로 회전 3D 프린팅함으로써 이중 변형이 가능한 스텐트를 제작하였다. 본 연구에서는 35oC와 55oC로 형상 복원온도가 다른 SMP를 활용함으로써 시술 후 온도 상승에 따라 두 단계에 걸쳐 형상 변형이 이루어질 수 있도록 하였다. SMP 재료의 배치 구성에 따라 길이 방향으로 두 단계의 변형이 이루어지거나 길이방향 및 원주방향의 두 단계로 변형이 이루어질 수 있도록 구현하였다. 이러한 3D 프린팅 기반의 형상변형 특징을 갖는 스텐트는 심혈관계 질환의 스텐트 시술에 있어 최소침습형으로 활용할 수 있으며 병변 부위 접근 방식 및 치료 방식을 다변화하여 환자맞춤형 치료에 다양하게 기여할 수 있을 것으로 기대된다.
Acknowledgments
본 연구는 2022년도 부산대학교 기계기술연구원의 연구회 지원사업 연구비 지원으로 이루어졌음(No. PNU RIMT2022-01(CMIT2022-19)).
REFERENCES
-
Gibson, I., Rosen, D. W., Stucker, B., Khorasani, M., Rosen, D., Stucker, B., Khorasani, M., (2021), Additive manufacturing technologies, Springer.
[https://doi.org/10.1007/978-3-030-56127-7]

- Wohlers, T., Caffrey, T., (2010), Wohlers report 2010, Wohlers Associates. https://wohlersassociates.com/product/wohlers-report-2010/
-
Zhou, L. Y., Fu, J., He, Y., (2020), A review of 3D printing technologies for soft polymer materials, Advanced Functional Materials, 30(28), 2000187.
[https://doi.org/10.1002/adfm.202000187]

-
Goh, G. D., Yap, Y. L., Tan, H., Sing, S. L., Goh, G. L., Yeong, W. Y., (2020), Process–structure–properties in polymer additive manufacturing via material extrusion: A review, Critical Reviews in Solid State and Materials Sciences, 45(2), 113-133.
[https://doi.org/10.1080/10408436.2018.1549977]

-
Tang, K., Ma, H., Tian, Y., Liu, Z., Jin, H., Hou, S., Zhou, K., Tian, X., (2020), 3D printed hybrid-dimensional electrodes for flexible micro-supercapacitors with superior electrochemical behaviours, Virtual and Physical Prototyping, 15(sup1), 511-519.
[https://doi.org/10.1080/17452759.2020.1842619]

-
Liu, H., Zhou, H., Lan, H., Liu, T., (2017), Organ regeneration: Integration application of cell encapsulation and 3D bioprinting, Virtual and Physical Prototyping, 12(4), 279-289.
[https://doi.org/10.1080/17452759.2017.1338065]

-
Zhao, Q., Qi, H. J., Xie, T., (2015), Recent progress in shape memory polymer: New behavior, enabling materials, and mechanistic understanding, Progress in Polymer Science, 49, 79-120.
[https://doi.org/10.1016/j.progpolymsci.2015.04.001]

-
Liu, C., Qin, H., Mather, P., (2007), Review of progress in shape-memory polymers, Journal of Materials Chemistry, 17(16), 1543-1558.
[https://doi.org/10.1039/b615954k]

-
Hager, M. D., Bode, S., Weber, C., Schubert, U. S., (2015), Shape memory polymers: Past, present and future developments, Progress in Polymer Science, 49, 3-33.
[https://doi.org/10.1016/j.progpolymsci.2015.04.002]

-
Sokolowski, W., Metcalfe, A., Hayashi, S., Raymond, J., (2007), Medical applications of shape memory polymers, Biomedical Materials, 2(1), S23.
[https://doi.org/10.1088/1748-6041/2/1/S04]

-
Holman, H., Kavarana, M. N., Rajab, T. K., (2021), Smart materials in cardiovascular implants: Shape memory alloys and shape memory polymers, Artificial Organs, 45(5), 454-463.
[https://doi.org/10.1111/aor.13851]

-
Brancati, M. F., Burzotta, F., Trani, C., Leonzi, O., Cuccia, C., Crea, F., (2017), Coronary stents and vascular response to implantation: Literature review, Pragmatic and Observational Research, 137-148.
[https://doi.org/10.2147/POR.S132439]

-
Jeewantha, L. H. J., Epaarachchi, J. A., Forster, E., Islam, M., Leng, J., (2022), Early research of shape memory polymer vascular stents, Express Polymer Letters, 16(9), 902-923.
[https://doi.org/10.3144/expresspolymlett.2022.66]

-
Ang, H. Y., Huang, Y. Y., Lim, S. T., Wong, P., Joner, M., Foin, N., (2017), Mechanical behavior of polymer-based vs. metallic-based bioresorbable stents, Journal of Thoracic Disease, 9(Suppl 9), S923.
[https://doi.org/10.21037/jtd.2017.06.30]

-
Lin, C., Zhang, L., Liu, Y., Liu, L., Leng, J., (2020), 4D printing of personalized shape memory polymer vascular stents with negative Poisson’s ratio structure: A preliminary study, Science China Technological Sciences, 63(4), 578-588.
[https://doi.org/10.1007/s11431-019-1468-2]

-
Reeser, K., Doiron, A. L., (2019), Three-dimensional printing on a rotating cylindrical mandrel: A review of additive-lathe 3D printing technology, 3D Printing and Additive Manufacturing, 6(6), 293-307.
[https://doi.org/10.1089/3dp.2019.0058]

-
Smith, M. L., Jones, J. F., (2018), Dual-extrusion 3D printing of anatomical models for education, Anatomical Sciences Education, 11(1), 65-72.
[https://doi.org/10.1002/ase.1730]

- Bhullar, S., Ko, J., Ahmed, F., Jun, M., (2014), Design and fabrication of stent with negative Poisson’s ratio, International Journal of Mechanical and Mechatronics Engineering, 8(2), 448-454.
-
Raamachandran, J., Jayavenkateshwaran, K., (2007), Modeling of stents exhibiting negative Poisson’s ratio effect, Computer Methods in Biomechanics and Biomedical Engineering, 10(4), 245-255.
[https://doi.org/10.1080/10255840701198004]

-
Zhao, W., Zhang, F., Leng, J., Liu, Y., (2019), Personalized 4D printing of bioinspired tracheal scaffold concept based on magnetic stimulated shape memory composites, Composites Science and Technology, 184, 107866.
[https://doi.org/10.1016/j.compscitech.2019.107866]

-
Omid, S. O., Goudarzi, Z., Kangarshahi, L. M., Mokhtarzade, A., Bahrami, F., (2020), Self-expanding stents based on shape memory alloys and shape memory polymers, Journal of Composites and Compounds, 2(3), 92-98.
[https://doi.org/10.29252/jcc.2.2.5]


M.S. candidate in the Department of Mechanical Engineering, Pusan National University. His research interest is additive manufacturing and artificial intelligence.
E-mail: yuseok@pusan.ac.kr

M.S. student in the Department of Mechanical Engineering, Pusan National University. His research interest is additive manufacturing and artificial intelligence.
E-mail: ch273404@pusan.ac.kr

Associate Professor in School of Mechanical Engineering, Pusan National University. His research interest is manufacturing of biomedical system and AI-based additive manufacturing.
E-mail: selome815@pusan.ac.kr